国际顶级期刊Cell(IF:66.8)2026年4月刊重磅刊发综述“Hallmarks of cancer-Then and now, and beyond”,以系统性框架整合近26年癌症研究成果,将癌症特征凝练为四大核心维度,为解析恶性肿瘤的发生发展、异质性及治疗耐药机制提供了全新理论范式。
这一版综述是Douglas Hanahan教授对“癌症特征”系列的第四次关键更新与升华。继2000年与Robert A. Weinberg教授在Cell发表首版、2011年更新至10项特征、2022年加入“解锁表型可塑性”这一第九项特征后,Hanahan教授此次进一步整合了肿瘤神经支配、多态微生物组等近十年的重要发现,构建了包含9项获得性功能特征、5项表型赋能特征、7类肿瘤微环境特征介导细胞及系统性相互作用的四维框架,使这一经典理论既保持了核心逻辑的连贯性,又全面覆盖了癌症研究的前沿进展。
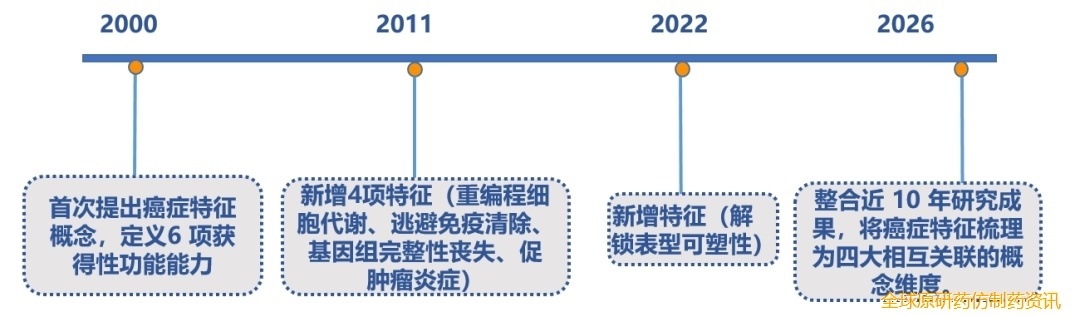
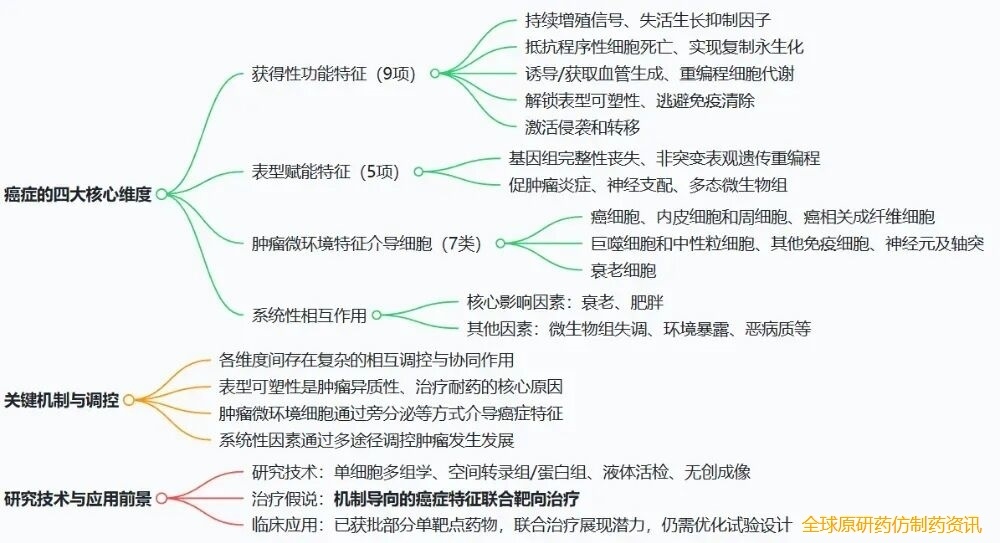
这是癌症细胞在肿瘤发生、发展和进化中逐步获得的核心能力,是癌症的本质特征,各特征并非线性获得,其出现顺序因肿瘤类型和起源细胞而异,核心内容如下:
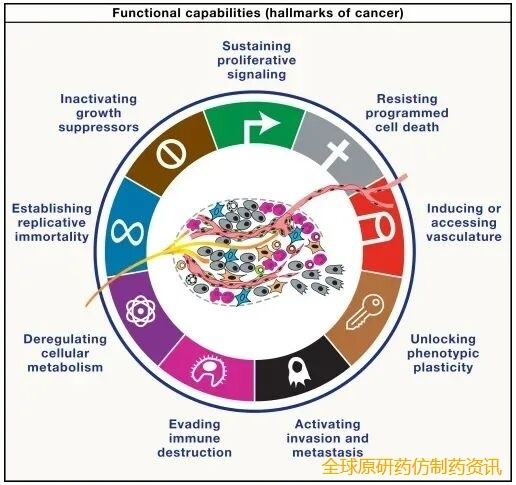
特征名称 | 核心机制 | 典型案例 |
持续增殖信号 | 癌基因(KRAS、MYC等)突变/扩增,自分泌/旁分泌生长因子 | KRAS突变见于~30% 人类肿瘤,MYC异常见于40%人类肿瘤 |
失活生长抑制因子 | 抑癌基因(TP53、RB、APC 等)突变失活,旁分泌生长抑制机制被绕开 | TP53突变见于~40%人类肿瘤,60%-70% 为错义突变 |
抵抗程序性细胞死亡 | 上调抗凋亡蛋白(BCL-2 等),TP53 失活,多种死亡通路被抑制 | BCL-2抑制剂维奈托克获批用于白血病治疗 |
实现复制永生化 | 端粒酶(TERT)激活或端粒替代延长(ALT),突破复制衰老限制 | TERT启动子突变见于~15%人类肿瘤,胶质母细胞瘤中达~80% |
诱导/获取血管生成 | 分泌促血管生成因子(VEGFA等),或共选择正常血管 | 肿瘤血管存在血管生成和血管共选择两种方式 |
重编程细胞代谢 | 采用有氧糖酵解+氧化磷酸化的混合代谢,利用谷氨酰胺等替代燃料 | 癌相关成纤维细胞与癌细胞存在代谢共生关系 |
解锁表型可塑性 | 谱系内/跨谱系可塑性,上皮-间质可塑性(EMP),癌症干细胞状态转换 | TP53 失活可促进去分化和谱系可塑性 |
逃避免疫清除 | T细胞耗竭,肿瘤微环境免疫抑制,抑制淋巴细胞浸润和活化 | 免疫检查点抑制剂(ICIs)可逆转T细胞耗竭 |
激活侵袭和转移 | 转移级联反应,形成预转移微环境,癌细胞休眠与复苏 | 转移是癌症发病和死亡的主要原因,部分癌细胞可休眠数十年 |
并非癌症的功能能力,而是癌细胞和肿瘤微环境中出现的异常表型,为癌症获得上述9项核心特征提供条件和支撑,是肿瘤发生发展的“助推器”:
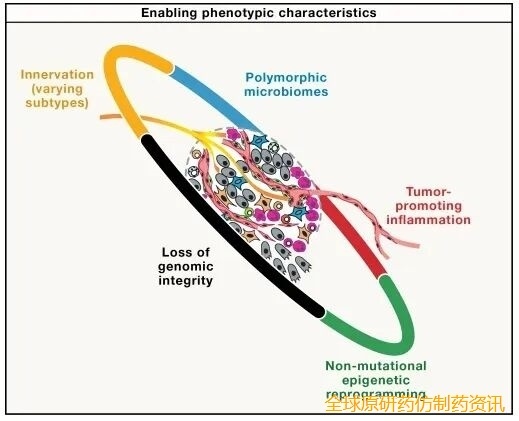
基因组完整性丧失:包括点突变、染色体畸变、ecDNA形成等,端粒功能异常加剧基因组不稳定性,超750个基因被证实为癌基因/抑癌基因;
非突变表观遗传重编程:通过DNA甲基化、组蛋白修饰等调控基因表达,是表型可塑性的核心驱动因素,部分儿科肿瘤无驱动基因突变,仅由表观遗传调控;
促肿瘤炎症:先天免疫细胞浸润,模拟伤口愈合的炎症微环境,介导增殖、血管生成等多项癌症特征,被称为“永不愈合的伤口”;
神经支配:肿瘤内交感/副交感神经及感觉神经的轴突投射,通过神经递质调控癌症特征,部分肿瘤存在神经元-癌细胞突触连接;
多态微生物组:肠道等部位的微生物组组成差异,调控肿瘤免疫微环境,粪菌移植可逆转免疫治疗耐药。
肿瘤并非单一癌细胞的集合,而是由癌细胞和多种招募/重编程的正常细胞组成的“细胞生态系统”,这些异质性细胞被称为“犯罪帮凶”,直接介导癌症的各项核心特征,且几乎所有细胞都存在多种表型状态:
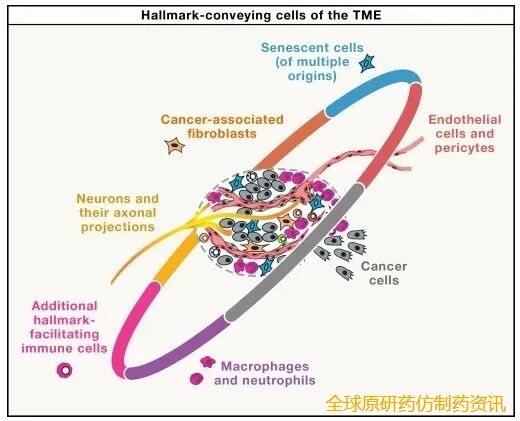
· 癌细胞:核心细胞,携带遗传/表观遗传异常,存在肿瘤内异质性和癌症干细胞(CSC)状态,超750个突变基因参与其表型调控;
· 内皮细胞和周细胞:构成肿瘤血管,调控血管生成、免疫细胞浸润,其异常是肿瘤免疫抑制的重要原因;
· 癌相关成纤维细胞(CAFs):分为肌成纤维细胞型、炎症型等,参与基质重塑、代谢共生、免疫抑制;
· 巨噬细胞和中性粒细胞:肿瘤相关巨噬细胞(TAMs)、中性粒细胞(TANs)存在促肿瘤/抑肿瘤表型,是促肿瘤炎症的核心细胞;
· 其他免疫细胞:包括树突状细胞、NK细胞、调节性T/B细胞(Treg/Breg)等,多呈现免疫抑制表型;
· 神经元及轴突:新增的TME细胞类型,通过神经递质和突触连接调控癌细胞增殖、转移等;
· 衰老细胞:通过衰老相关分泌表型(SASP)介导促肿瘤炎症,参与调控癌细胞增殖和免疫抑制。
肿瘤是全身性疾病,与机体的循环、神经、微生物组等系统存在复杂的相互作用,多种系统性因素调控癌症的各项特征,文中重点阐释了两大核心影响因素:
衰老:与癌症发病率正相关,衰老组织积累致癌突变、衰老细胞,免疫功能衰退,细胞表型可塑性增加,且“衰老特征”与癌症特征高度重叠;
肥胖:通过脂肪细胞分泌的瘦素/脂联素失衡,调控癌细胞增殖、血管生成、代谢重编程,与多种癌症的发病风险相关。
此外,环境暴露(吸烟、污染)、肿瘤诱导的恶病质、微生物组失调等也属于系统性相互作用的范畴。
多组学技术:单细胞RNA/DNA/蛋白测序、空间转录组/蛋白组,助力解析肿瘤内异质性和癌症特征的空间分布;
无创检测技术:液体活检(检测循环肿瘤细胞/分子)、无创成像,实现癌症特征的动态监测,弥补活检的局限性;
生物信息学技术:机器学习、人工智能,用于整合多组学数据,构建“数字病理模型”,解析癌症特征的调控网络。
单靶点治疗的局限性:目前仅获批针对增殖信号、血管生成、免疫清除等5项特征的药物,多数单药治疗会出现适应性耐药;
联合靶向治疗的核心逻辑:同时靶向不同的癌症特征、表型赋能特征或TME介导细胞,利用“多重靶向”提高癌症的耐药门槛,延长治疗效果;
已获批的联合治疗案例:
VEGF/VEGFR抑制剂+ ICIs:靶向血管生成和免疫清除,获批用于肾癌、肺癌等;
抗VEGF单抗+ PARP抑制剂:靶向血管生成和基因组完整性丧失,获批用于卵巢癌;
BCL-2抑制剂+表观遗传药物:靶向细胞死亡抵抗和表观遗传重编程,获批用于急性髓系白血病;
潜在的联合治疗策略:ICIs联合TME免疫抑制细胞重编程药物,逆转肿瘤微环境的免疫抑制状态。
[1] Hanahan D. Hallmarks of cancer-Then and now, and beyond. Cell. 2026 Jan 29:S0092-8674(25)01498-9. doi: 10.1016/j.cell.2025.12.049. Epub ahead of print.
生成海报
 长按扫码关注公众号
长按扫码关注公众号