
2026年3月19日发表于 barw medical journal
摘要
介绍
Tarlatamab 是一种靶向 Delta 样配体 3 (DLL3) 的双特异性 T 细胞衔接器,近期获批用于治疗铂类化疗后进展的晚期小细胞肺癌 (SCLC) 患者。本荟萃分析评估了 tarlatamab 单药治疗及联合治疗方案在 SCLC 治疗中的疗效和安全性。
方法
本研究按照PRISMA 2020指南进行了系统评价和荟萃分析。检索了PubMed/MEDLINE和EMBASE数据库,检索时间从建库至2025年9月,以识别评估tarlatamab治疗小细胞肺癌(SCLC)的临床试验。纳入的研究需报告可量化的疗效和/或安全性结果。采用随机效应模型合并客观缓解率(ORR)和疾病控制率(DCR),并应用Kaplan-Meier法评估生存结局。
结果
本研究纳入了7项临床试验,共涉及1247例晚期小细胞肺癌(SCLC)患者。汇总客观缓解率(ORR)为0.42(95% CI 0.31–0.54),单药治疗研究的缓解率范围为21%至47%,联合治疗方案的缓解率最高可达48%。在6项研究中,汇总疾病控制率(DCR)为0.48(95% CI 0.31–0.66),联合治疗方案的DCR最高可达87%。中位无进展生存期(PFS)为3.5至5.6个月,中位总生存期(OS)为13.2至25.3个月。汇总生存分析显示,疾病进展和死亡风险显著降低。3级和4级不良事件的发生率分别为5.4%和1.4%,但部分研究的安全性报告不完整。
结论
Tarlatamab 在既往接受过大量治疗的小细胞肺癌 (SCLC) 患者中展现出具有临床意义的抗肿瘤活性,且安全性良好。这些发现支持将 DLL3 靶向疗法作为一种有前景的治疗策略,并值得开展进一步的前瞻性研究,以明确其在不断发展的 SCLC 治疗格局中的最佳作用。
介绍
小细胞肺癌(SCLC)是最具侵袭性和致死率的肺部恶性肿瘤之一,约占所有肺癌病例的13%至17%。其特点是肿瘤生长迅速、早期扩散以及极易产生耐药性,这些因素共同导致诊断和治疗的复杂性。对于局限期患者,标准治疗方案为联合治疗,采用以铂类为基础的化疗,最常用的是顺铂或卡铂联合依托泊苷,并同时进行胸部放疗。对于达到完全缓解的患者,通常会进行预防性颅脑照射以降低中枢神经系统转移的风险。
在广泛期小细胞肺癌(SCLC)中,治疗策略已扩展至包括免疫疗法,特别是程序性死亡配体1 ( PD-L1)抑制剂,并联合传统化疗。尽管取得了这些进展,但由于耐药性的快速发展、频繁复发以及显著的治疗相关毒性,长期生存率仍然很低。虽然免疫检查点抑制剂(ICIs)已在多种恶性肿瘤中改变了预后,但其在SCLC中的疗效有限。尽管SCLC的高肿瘤突变负荷提示其可能对免疫疗法敏感,但仅有部分患者能从一线化疗联合ICIs中获益。这种疗效有限的原因包括主要组织相容性复合体(MHC)分子表达降低、抗原呈递受损以及显著的肿瘤内异质性。然而,大型国际试验表明,在化疗中加入PD-L1抑制剂(包括度伐利尤单抗)可提高生存率,这支持了化疗免疫疗法在小细胞肺癌中的作用。早期证据表明,肿瘤免疫原性较强的患者可能是这些联合疗法的主要受益者。
鉴于现有疗法的局限性,小细胞肺癌(SCLC)亟需新的治疗策略。分子特征分析和对SCLC生物学理解的进展,使得靶向疗法的开发成为可能,旨在克服疾病进展和治疗耐药性,并提升了个体化治疗的潜。Tarlatamab是一种双特异性T细胞衔接器(BiTE)免疫疗法,靶向肿瘤细胞上的delta样配体3(DLL3)。
细胞和T细胞上的CD3受体,导致T细胞活化、细胞因子释放,并对表达DLL3的癌细胞产生选择性细胞毒性。基于DeLLphi-301 II期临床试验中观察到的持久抗肿瘤活性和可控的安全性,tarlatamab于2024年5月获得美国食品药品监督管理局(FDA)加速批准,用于治疗铂类化疗后疾病进展的广泛期小细胞肺癌(SCLC)患者。本荟萃分析评估了tarlatamab作为单药治疗以及与其他疗法联合治疗SCLC的疗效和安全性。
方法
研究设计与设置
本系统评价和荟萃分析综合了评估tarlatamab治疗小细胞肺癌(SCLC)疗效的临床试验证据。治疗方案分为四组:A组为tarlatamab单药治疗,B组为tarlatamab联合化疗,C组为tarlatamab联合PD-L1抑制剂atezolizumab,D组为tarlatamab联合PD-L1抑制剂durvalumab。所有方法和报告均遵循2020年系统评价和荟萃分析的首选报告条目(PRISMA)指南。
数据来源和搜索策略
我们对 PubMed/MEDLINE 和 EMBASE 数据库进行了全面的检索,检索范围从建库至 2025 年 9 月,旨在识别评估 tarlatamab 治疗小细胞肺癌 (SCLC) 的临床试验和观察性研究。为了最大限度地提高检索灵敏度,我们使用了截词符和通配符检索。检索未设语言限制。此外,我们还手工检索了相关的期刊文章和临床试验注册库,以识别其他研究。
纳入标准
符合以下条件的研究可纳入本研究:(1) 评估 tarlatamab 单药治疗或联合治疗方案;(2) 报告可量化的临床结局,包括缓解率、总生存期 (OS)、无进展生存期 (PFS) 或疾病进展时间;(3) 纳入既往接受过铂类化疗或其他全身治疗的广泛期或局限期患者。评估 tarlatamab 作为二线、三线或后续治疗方案的研究也符合纳入标准。
排除标准
如果符合以下条件,则排除研究:(1)不是临床试验;(2) 没有重点关注 tarlatamab 治疗 SCLC;(3)呈现重叠或重复的患者人群;(4)缺乏足够的疗效或安全性数据;(5)以英语以外的语言发表;(6)是预印本、仅摘要报告或发表在掠夺性期刊上。
研究选择过程
两位独立的研究人员根据预先设定的纳入和排除标准筛选了所有检索到的研究的标题和摘要。所有可能符合纳入标准的文章均由两位研究人员进行全文审阅。任何关于研究纳入资格的分歧均通过讨论达成共识。
数据项
从符合纳入标准的研究中提取的数据包括:(1)研究和患者特征(第一作者姓名、发表年份、样本量、试验阶段);(2)人口统计学变量(中位年龄、性别分布、吸烟状况);(3)临床基线特征(ECOG 体能状态、转移部位、既往铂类化疗、既往治疗线数、既往免疫治疗暴露、既往放疗);(4)治疗详情(tarlatamab 剂量、给药频率、治疗中位持续时间);(5)不良事件数据(根据不良事件通用术语标准 [CTCAE] 分级,包括 1-5 级事件和严重不良事件);以及(6)临床疗效结果(缓解率、疾病控制率、无进展生存期和总生存期)。
数据分析与综合
数据提取和整理使用 Microsoft Excel (2019)。描述性统计分析采用 SPSS 26.0 版进行,结果以频数、百分比、中位数和范围表示。采用 Meta 分析综合疗效指标。对于二分类结局(客观缓解率和疾病控制率),使用 METAANALYSISONLINE 生成森林图以可视化合并效应估计值和异质性。对于生存时间结局(无进展生存期和总生存期),采用 Kaplan-Meier 法估计中位生存期,并使用 Brookmeyer 和 Crowley 方法计算 95% 置信区间 (CI) 。
结果
研究选择
对同行评审数据库进行系统检索,初步筛选出214篇与tarlatamab和小细胞肺癌相关的潜在文献。去除重复文献(n=2)、非英文文献(n=2)以及仅有摘要的文献(n=9)后,对剩余的201篇文献进行标题和摘要筛选。筛选出188篇文献进行全文审阅。应用预先设定的纳入标准,最终筛选出14篇文献进行详细评估。其中,7篇文献因预印本(n=4)或发表于掠夺性期刊(n=3)而被排除,最终纳入7项符合条件的临床试验进行荟萃分析[16-22]。PRISMA流程图展示了完整的文献筛选过程(图1)。所有纳入的参考文献均经过审查,以排除未经同行评审的数据。
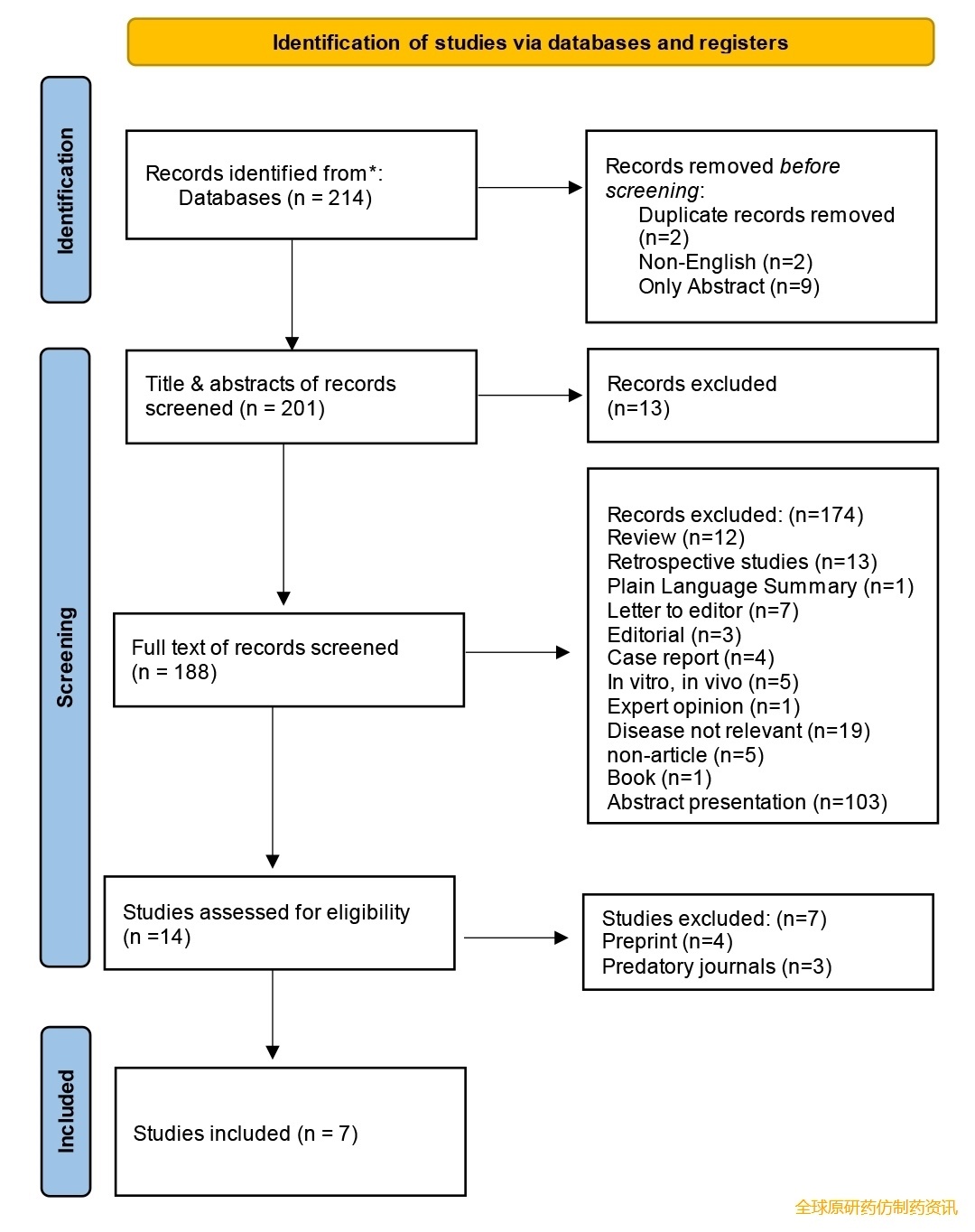
图1 研究选择PRISMA流程图
患者特征
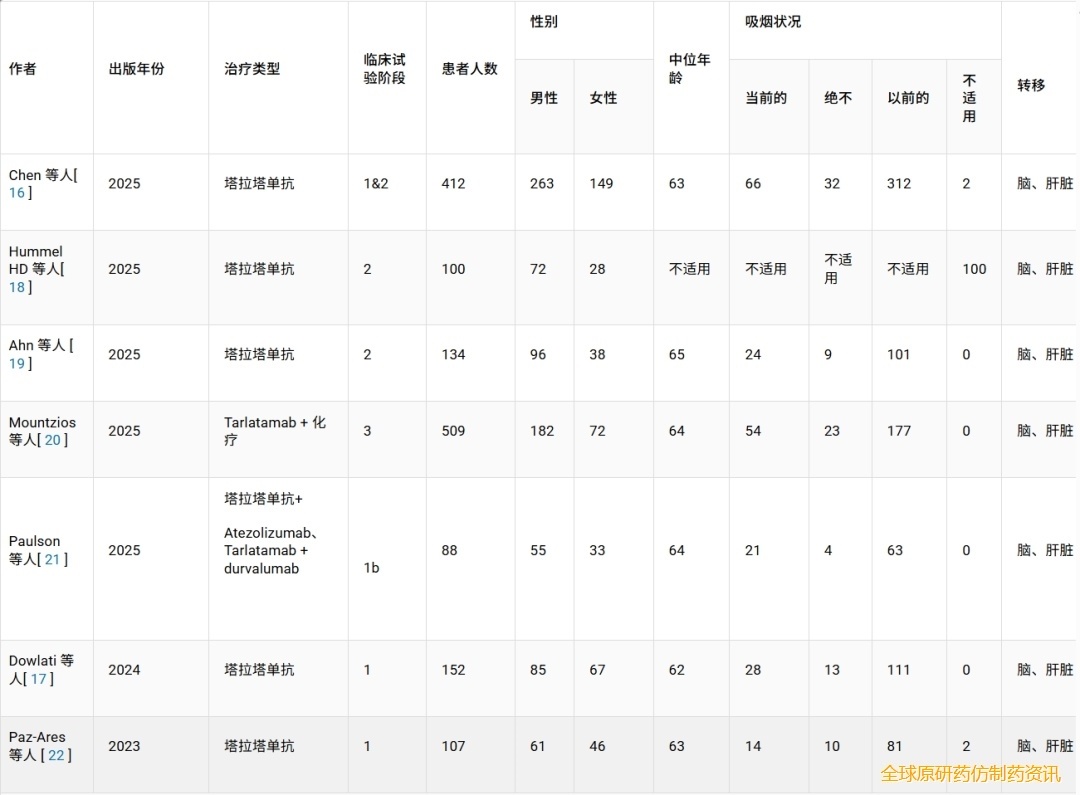
在纳入的七项临床试验中,基线研究层面的特征表明,晚期小细胞肺癌患者人群相对同质。大多数研究为早期试验,评估了tarlatamab单药治疗或联合治疗方案的疗效。试验层面的中位年龄为62至65岁,男性患者在各研究中均占多数。脑转移和肝转移是所有试验中最常见的转移部位(表1)。
表1 参与小细胞肺癌临床试验的患者的基线特征
共有1247例患者纳入分析。患者的中位年龄为63.5岁。男性患者814例(65.3%),女性患者433例(34.7%)。大多数患者报告了吸烟史,其中既往吸烟者占比最大(845例,67.8%),其次是目前吸烟者(207例,16.6%)和从不吸烟者(91例,7.3%)。104例患者(8.3%)未报告吸烟史。与试验层面的结果一致,转移性病变最常累及脑和肝脏(表2)。
表2 患者人口统计学特征、既往治疗史和治疗反应
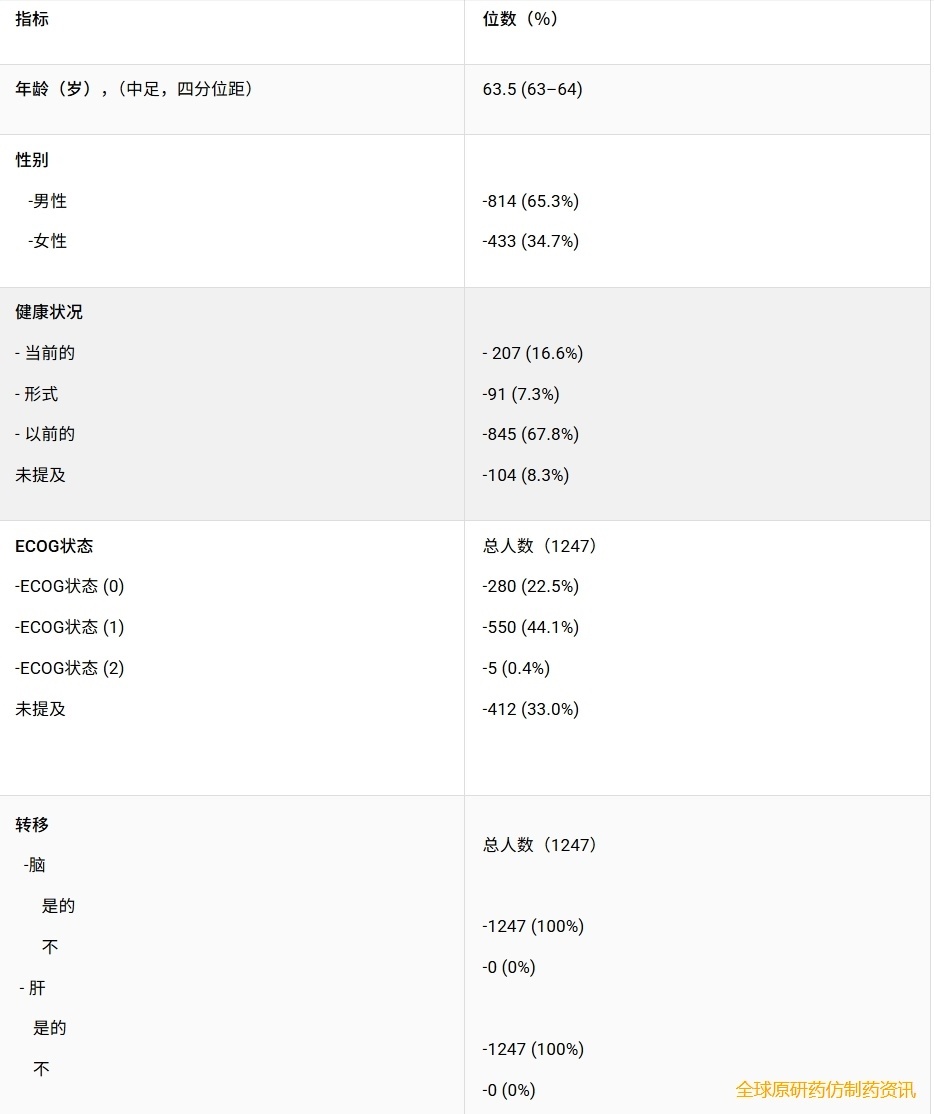
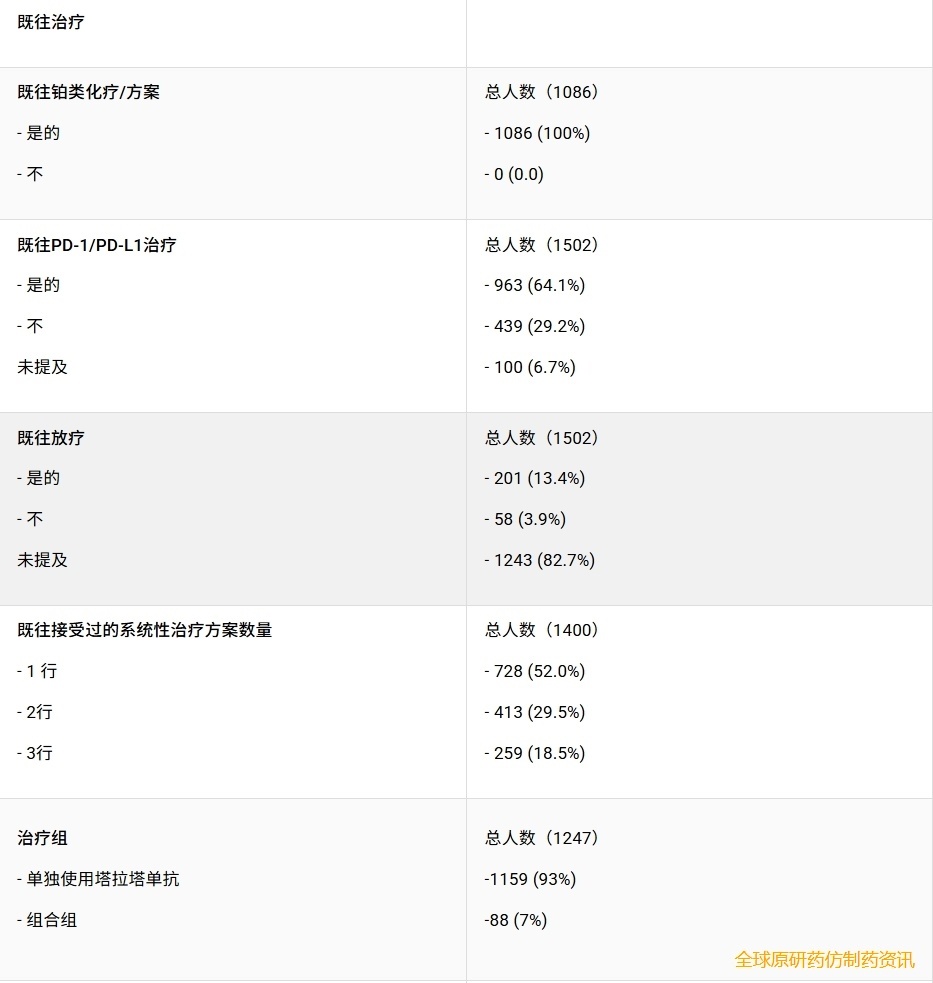
既往治疗和体能状态
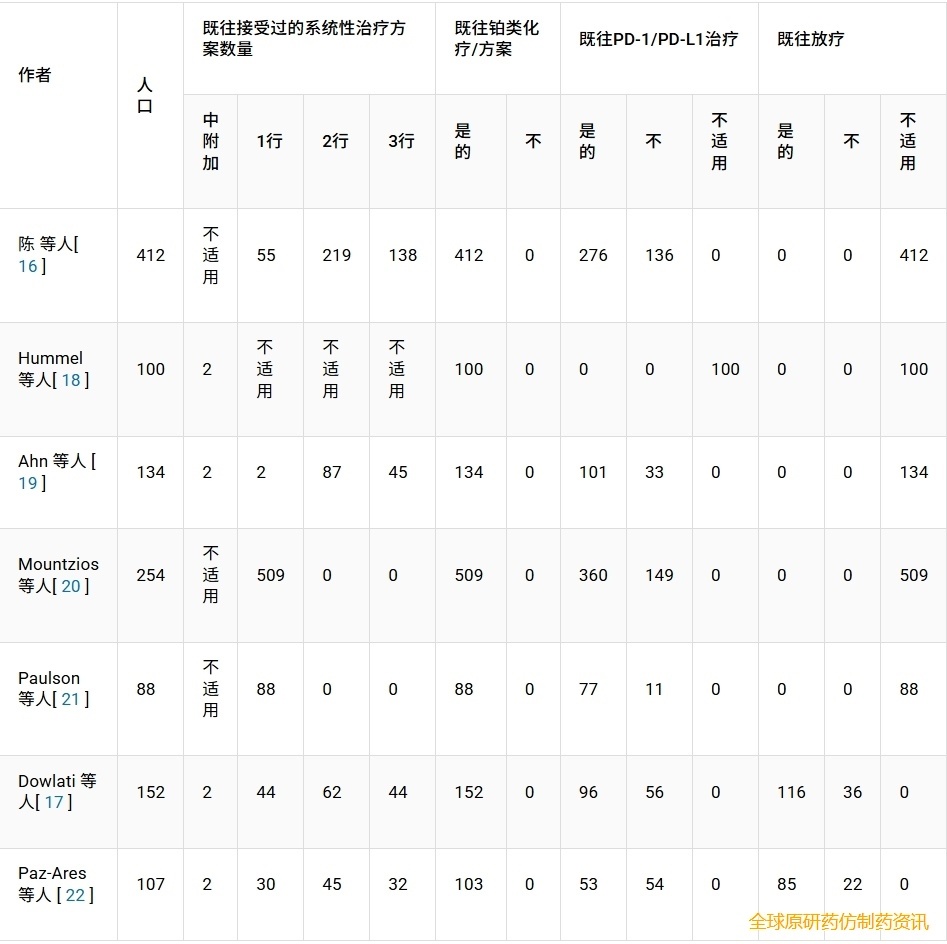
所有患者均接受过铂类化疗。大多数患者接受过一线全身治疗(728 例,52.0%),其次是两线治疗(413 例,29.5%)和三线治疗(259 例,18.5%)。963 例患者(64.1%)既往接受过 PD-1 或 PD-L1 抑制剂治疗,而 439 例患者(29.2%)未接受过免疫治疗。201 例患者(13.4%)有既往放疗史。在报告了美国东部肿瘤协作组(ECOG)体能状态评分的患者中,280 例(22.5%)ECOG 评分为 0 分,550 例(44.1%)评分为 1 分,5 例(0.4%)评分为 2 分。412 例患者(33.0%)未报告 ECOG 体能状态评分(表 2 和表 3)。
表3 肺癌患者的既往治疗方案
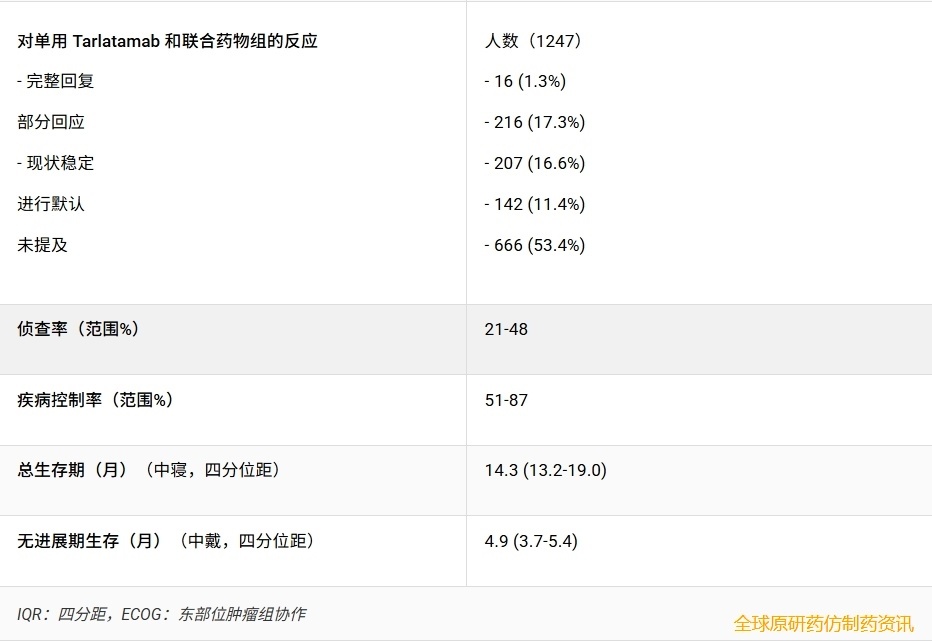
疗效结果
在纳入的七项研究中,疾病反应采用实体瘤疗效评价标准(RECIST)或研究者定义的标准进行评估。在可评估人群(n=1247)中,16例患者(1.3%)达到完全缓解,216例患者(17.3%)达到部分缓解,207例患者(16.6%)病情稳定,142例患者(11.4%)病情进展。666例患者(53.4%)未报告或无法评估疗效,主要原因是研究提前终止、缺乏基线后影像学检查或根据试验方案被归类为不可评估(表2)。
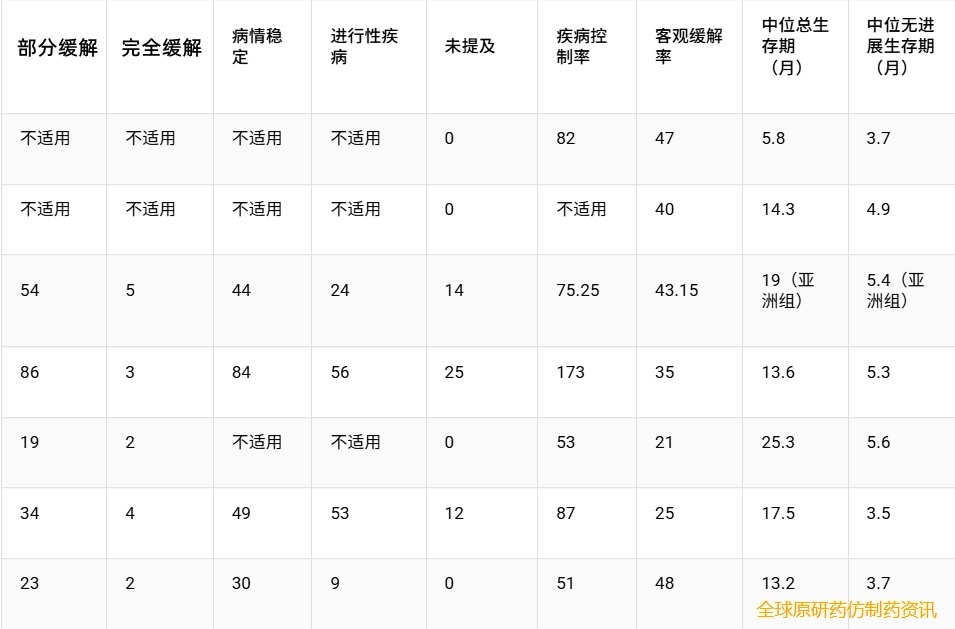
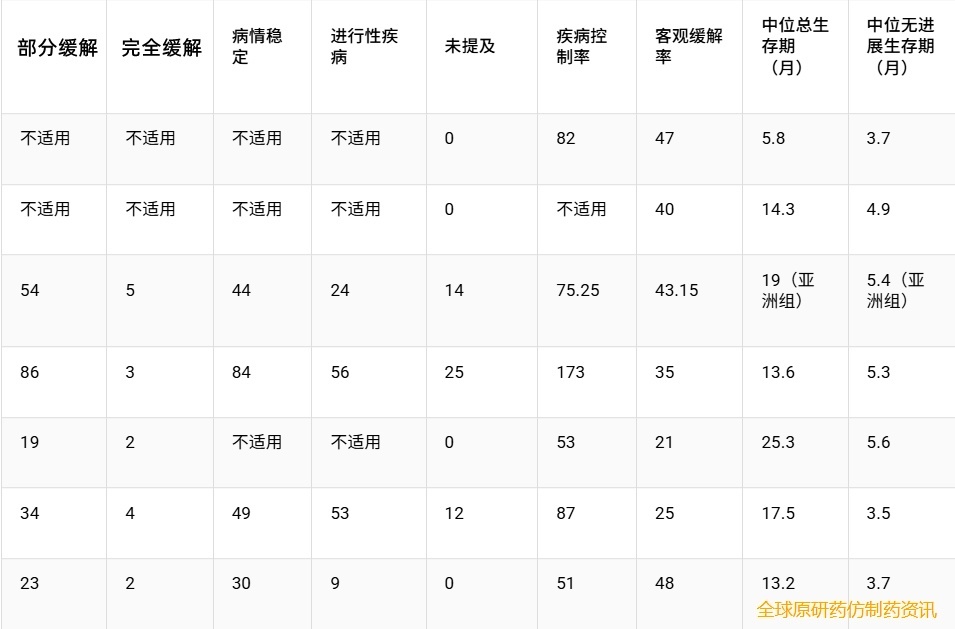
在评估tarlatamab单药治疗的研究中,疾病控制率(DCR)为51%至82%,客观缓解率(ORR)为21%至47%。在评估联合治疗的研究中,观察到更高的缓解率,DCR最高达87%,ORR最高达48%。各研究报告的中位无进展生存期(PFS)为3.5至5.6个月,中位总生存期(OS)为13.2至25.3个月。在亚洲亚组中,中位OS达到19.0个月,中位PFS为5.4个月(表4)。
表4 Tarlatamab 单药治疗和联合治疗的临床结果
森林图展示了各研究的客观缓解率估计值及其对应的95%置信区间(CI),这些估计值采用随机效应模型进行合并。每个方块的大小代表该研究在荟萃分析中的权重,水平线表示95%置信区间。菱形代表合并后的客观缓解率及其95%置信区间。图中还显示了一个预测区间,以反映未来研究中预期的治疗效果范围。各研究间存在显著的异质性(I² = 94.6%,P<0.0001)(图2)。
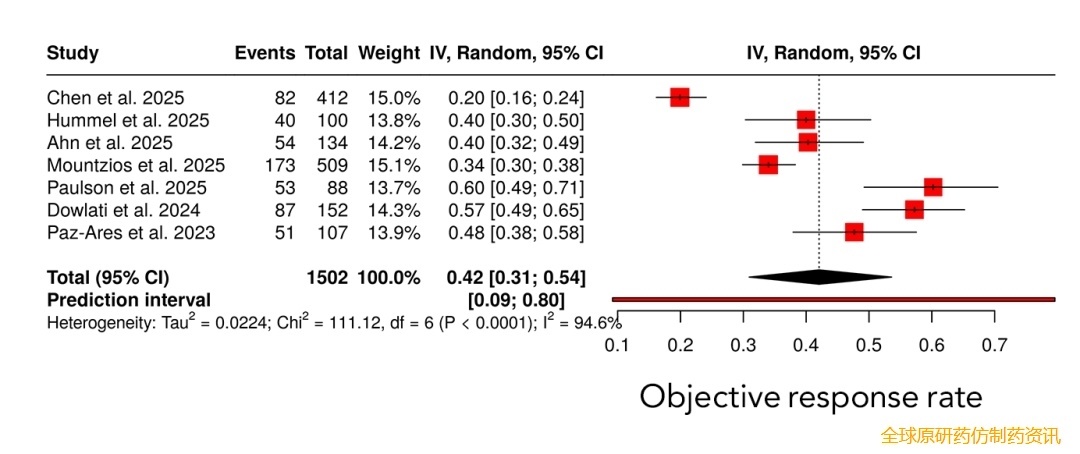
图2 复发性小细胞肺癌患者接受tarlatamab治疗的汇总客观缓解率(ORR)森林图
在包含 1402 例患者的六项研究中,汇总的疾病控制率 (DCR) 估计值为 0.48(95% CI 0.31–0.66)。存在显著的异质性,I² 值为 97.6%。预测区间为 0.02 至 0.97,反映了各研究间疾病控制结果的较大差异(图 3)。各研究的中位无进展生存期 (PFS) 存在差异,报告的中位值约为 3 至 6 个月。汇总的 Kaplan-Meier 分析显示风险比为 0.76,p 值为 0.003,具有统计学意义(如图所示)。各研究的中位总生存期 (OS) 约为 13 至 25 个月。汇总的 Kaplan-Meier 分析显示风险比为 0.71,p 值为 0.012。在长达 40 个月的随访期内,观察到各研究间生存轨迹的差异。(图 4)。
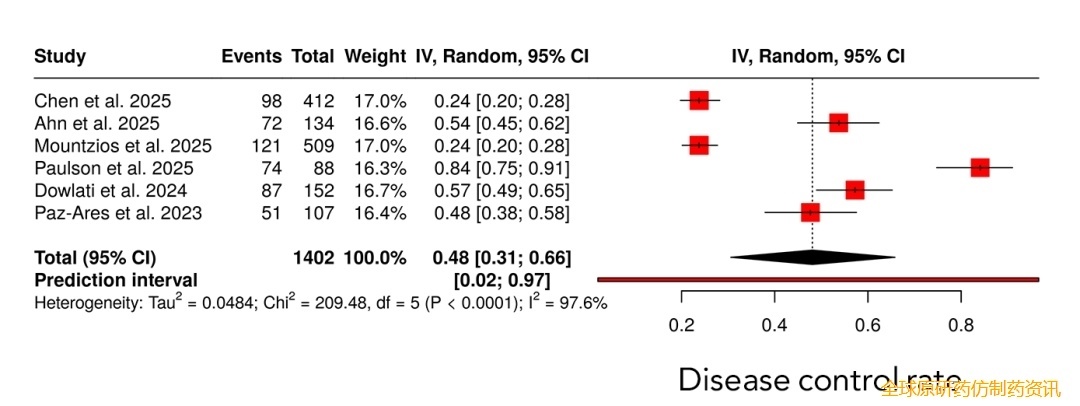
图3 复发性小细胞肺癌患者接受 tarlatamab 治疗后疾病控制率 (DCR) 的森林图
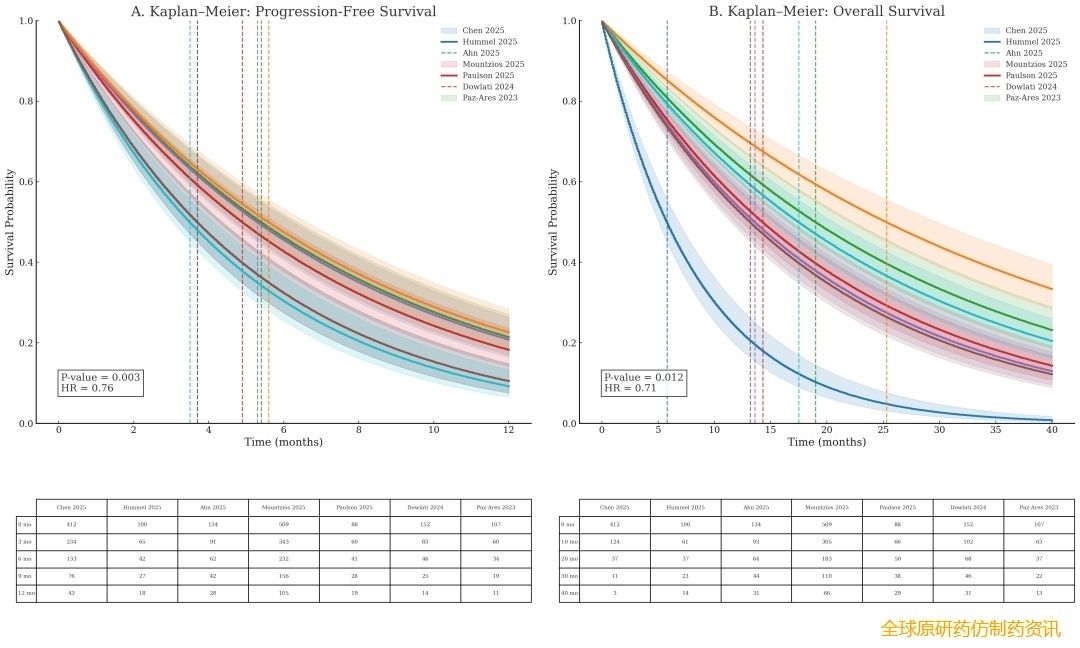
图4 Kaplan-Meier 估计 tarlatamab 治疗复发性小细胞肺癌的无进展生存期 (PFS) 和总生存期 (OS)
安全结果
在报告的人群中,136 例患者发生 2 级或以上不良事件,68 例患者(5.4%)发生 3 级不良事件,17 例患者(1.4%)发生 4 级不良事件。在有亚组特异性数据的研究中(包括亚洲人群),39 例患者报告发生 2 级或以上不良事件,24 例患者报告发生 3 级不良事件,7 例患者报告发生 4 级不良事件,2 例患者报告发生 5 级不良事件。在记录了严重不良事件的研究中,129 例患者报告发生严重不良事件。相当一部分患者的不良事件严重程度和分级未被报告,因此在安全性数据集中被归类为“不可用”(表 5)。
表5 Tarlatamab治疗小细胞肺癌的不良反应
讨论
小细胞肺癌仍然是最具侵袭性的实体恶性肿瘤之一,其特点是肿瘤增殖迅速、早期转移扩散以及生存预后持续差。尽管化疗联合免疫疗法取得了进展,但晚期小细胞肺癌仍难以治愈,大多数患者在接受一线铂类化疗后六个月内复发。铂类化疗失败后的预后尤其差,标准二线治疗方案如拓扑替康和鲁比替定的客观缓解率低于20%,中位总生存期很少超过10个月。这些有限的临床获益凸显了复发性小细胞肺癌治疗领域亟待满足的重大需求。因此,人们越来越关注寻找能够提供更持久疗效且安全性可接受的生物学靶点。在众多新兴靶点中,DLL3因其在小细胞肺癌肿瘤细胞上的高表达和选择性表达以及在正常组织中的极低表达而备受关注。这种肿瘤特异性表达模式为复发性小细胞肺癌中针对 DLL3 的治疗策略提供了强有力的生物学依据。
既往的前瞻性研究和真实世界研究一致表明,铂类化疗失败后复发的小细胞肺癌患者预后较差。Rudin 等人和 Paz-Ares 等人报道,采用拓扑替康和鲁比替定等标准二线治疗方案,客观缓解率通常低于 20%,中位总生存期很少超过 10 个月。这些结果凸显了该领域巨大的未满足治疗需求。相比之下,本荟萃分析显示,基于他拉单抗的治疗方案具有显著的临床疗效,汇总客观缓解率达 42%,疾病控制率在 51% 至 87% 之间,具体数值取决于治疗方案。值得注意的是,单药治疗和联合治疗均取得了优于既往报道的传统化疗的肿瘤缓解率。尽管应谨慎解读跨研究比较的结果,但与先前的文献相比,观察到的改善幅度支持了 tarlatamab 靶向 DLL3 治疗复发性小细胞肺癌的治疗潜力,并强调了进一步前瞻性验证的必要性。
基线时的转移负荷较大,与晚期小细胞肺癌相符。既往研究表明,脑和肝是小细胞肺癌最常见的转移部位,约40%~70%的患者在病程中会出现脑转移。与这些报道一致,脑和肝转移是本荟萃分析纳入试验中最常见的转移部位。广泛转移性疾病的存在反映了真实世界中晚期小细胞肺癌患者的情况,并增强了所观察到的治疗结果的外部有效性和普遍适用性。
体能状态是小细胞肺癌中公认的预后因素;然而,其对治疗结果的影响仍存在争议,尤其是在临床试验入组方面。Rudin等人和Paz-Ares等人已证实,ECOG评分较低的患者缓解率较低、无进展生存期较短、总生存期缩短,但这些患者在前瞻性试验中的代表性往往不足。在本荟萃分析中,大多数可评估患者的基线体能状态良好,其中22.5%的患者ECOG评分为0分,44.1%为1分,表明约三分之二的患者在接受治疗时功能状态良好。仅有少数患者的ECOG评分为2分(0.4%),而三分之一的病例未报告ECOG评分。这种不平衡凸显了关于基于试验的疗效估计的普遍性的持续争议,并表明当将治疗益处外推至功能储备较差的患者时,可能会高估治疗效果。
既往研究表明,铂类化疗失败后复发性小细胞肺癌患者的预后较差。Rudin等人、Paz-Ares等人、Dowlati等人以及Sands等人报道,拓扑替康和鲁比替定等标准二线治疗方案的客观缓解率通常低于20%,中位总生存期很少超过10个月。在此背景下,本荟萃分析表明,tarlatamab在既往接受过大量治疗的小细胞肺癌患者中具有临床意义的抗肿瘤活性。在1247例可评估疗效的患者中,完全缓解率和部分缓解率分别为1.3%和17.3%,汇总客观缓解率为42%。此外,近一半接受治疗的患者病情得到控制,联合治疗方案的疾病控制率高达87%,显著高于既往化疗的疗效水平。
生存结果进一步支持了这些发现的临床意义。中位无进展生存期为3.5至5.6个月,而中位总生存期在各研究中为13.2至25.3个月。Rudin等人、Paz-Ares等人、Dowlati等人和Sands等人一致报道,既往的二线治疗方案,如拓扑替康、鲁比替定和安柔比星,其中位总生存期约为5.8至10个月,凸显了这些方案在此类患者中疗效持续时间有限。与此相比,tarlatamab治疗后观察到的中位总生存期提高2至3倍,表明其在复发性小细胞肺癌中具有临床意义的生存优势。汇总生存分析进一步证实了疾病进展和死亡风险的统计学显著降低,无进展生存期和总生存期的风险比分别为0.76和0.71。值得注意的是,亚组分析表明,亚洲患者的中位总生存期约为19个月,与各试验报告一致,并支持了该疗法在不同人群中获益的可重复性。值得注意的是,在复发患者中,tarlatamab的生存结果接近甚至在某些研究中超过了一线化疗联合免疫治疗方案(如CASPIAN和KEYNOTE-604)的报道结果,这些方案的中位总生存期为12.3至13.0个月。尽管应谨慎解读跨试验比较结果,但考虑到小细胞肺癌(SCLC)治疗中疗效随治疗次数增加而递减的既定模式,在后续治疗中取得类似的生存结果尤其引人注目。
tarlatamab 的疗效在生物学上是合理的,并且与 DLL3 在小细胞肺癌发病机制中的既定作用相符。Ding 等人和 Zhang 等人已证实,DLL3 在神经内分泌型小细胞肺癌中高表达,并通过 Notch 信号通路的异常调控促进肿瘤增殖和维持。tarlatamab 通过同时激活 CD3 阳性 T 细胞和表达 DLL3 的肿瘤细胞,诱导强效的 T 细胞介导的细胞毒性,且该作用独立于主要组织相容性复合体 I 类限制性抗原呈递,从而绕过了小细胞肺癌特有的关键免疫逃逸机制,正如 Rudin 等人和 Paz-Ares 等人所强调的那样。这种作用机制明显区别于免疫检查点抑制剂,并可能解释了其在以往对免疫疗法反应有限的小细胞肺癌中表现出的强大抗肿瘤活性。
重要的是,与早期靶向DLL3的疗法(例如rovalpituzumab tesirine)相比,tarlatamab似乎具有更优的疗效和耐受性。Rudin等人和Paz-Ares等人报道,尽管rovalpituzumab tesirine显示出一定的缓解率,但未能改善生存期,并且在III期临床试验中伴有显著的毒性和较高的治疗中断率。相比之下,tarlatamab利用内源性免疫效应机制,无需递送细胞毒性有效载荷,从而提高了治疗指数并具有更佳的安全性,Rudin等人、Paz-Ares等人和Ding等人的研究结果均支持这一观点。
在纳入的研究中,tarlatamab 的耐受性总体良好。严重不良事件发生率较低,分别有 5.4% 和 1.4% 的患者报告了 3 级和 4 级毒性反应。最常见的治疗相关不良事件与 T 细胞衔接器疗法的预期特征一致,特别是细胞因子释放综合征,该综合征主要为低级别,且可通过标准支持措施快速逆转。Paz-Ares 等人和 Sands 等人报告称,神经毒性不常见且通常较轻,仅有少数患者出现 3-4 级事件。与传统细胞毒性化疗相比,这些结果表明 tarlatamab 在疗效和耐受性之间具有更佳的平衡。Rudin 等人开展的 III 期 DeLLphi-304 试验进一步证实了这一观察结果。与医生选择的化疗相比,tarlatamab 显示出显著更低的严重不良事件发生率和治疗中断率。
利用真实世界数据进行的间接治疗比较为这些发现提供了进一步的支持。Wang 等人报告称,在调整基线预后因素后,与真实世界中的对照疗法相比,tarlatamab 显著改善了患者的总生存期、无进展生存期和客观缓解率,这表明观察到的临床获益不仅限于临床试验的受控环境,还可能推广至更广泛的患者群体。汇总分析中观察到显著的异质性,反映了研究设计、治疗方案和患者特征的差异。在复发性小细胞肺癌的背景下,这种差异是预期的,反映了真实世界临床的复杂性。重要的是,tarlatamab 在异质性环境中的持续活性支持了其抗肿瘤作用的稳健性。基线肿瘤负荷较低、体能状态良好且无肝转移的患者似乎更有可能实现持续的疾病控制,这表明患者选择和早期干预可能优化治疗结果。应谨慎解读这些观察结果,并提出值得进一步前瞻性评估的假设性见解。
需要指出的是,本荟萃分析存在一些局限性。纳入的研究数量有限,其中许多是早期临床试验,且疗效指标存在显著的异质性。部分患者的疗效评估不完整,尤其是在剂量递增研究中,且各试验的安全性报告不一致。此外,由于缺乏个体患者数据,无法进行详细的亚组分析和生物标志物分析。这些局限性凸显了开展更多随机对照试验和生物标志物驱动型研究的必要性,以优化患者选择并确认tarlatamab在小细胞肺癌中的长期临床应用价值。
结论
这项荟萃分析揭示了靶向DLL3疗法作为晚期小细胞肺癌一种有前景的治疗策略的临床意义。研究结果表明,在标准治疗后治疗选择有限的背景下,tarlatamab展现出显著的抗肿瘤活性。重要的是,其疗效和耐受性之间的良好平衡支持了该疗法的持续临床开发。未来需要开展更多设计严谨的前瞻性研究,以明确tarlatamab在不断发展的小细胞肺癌治疗格局中的最佳定位。
点击“转发”吧
生成海报
 长按扫码关注公众号
长按扫码关注公众号