前言
NGS技术是精准医疗领域的关键技术,具有通量高、灵敏度高等优势,是乳腺肿瘤分子分型、遗传诊断、疗效监测、预后判断、耐药提示以及治疗方案选择的重要依据1。为助力临床医生将NGS报告有效转化为乳腺癌精准治疗方案,本文结合权威指南与临床研究,特邀中山大学孙逸仙纪念医院欧阳能太教授从报告质控、变异解读、治疗策略等关键环节系统梳理NGS报告解读路径,并通过虚拟病例案例进行“实战”分析,最终形成“检测—解读—决策—监测”的临床循证闭环,推动分子数据向患者实际获益转化。
根据《实体瘤常见驱动基因DNA和RNA高通量测序共检专家共识(2025版)》2,标准NGS报告应包括患者基本信息、检测结果、质控信息、变异解读等内容,还需要对检测的局限性及风险报告做必要的说明。
一、送检信息,确认报告是否“一对一”
标准NGS报告的基本信息通常包括:患者信息(如姓名、性别、年龄、住院号/门诊号等)、样本信息(如送检样本部位、送检时间、病理号/样本编号、检测样本类型等)、临床/病理诊断等2。
临床实践小tips:

基本信息在送检时应反复核对并填写完整,拿到NGS报告后再次核对。
二、检测结果,NGS报告“心脏重地”
临床实践小tips:

在核对基本信息无误后,再进行检测结果解读。
1.基因名称
中国乳腺癌患者常见基因突变发生频率:TP53(53%)、PIK3CA(44%)、AKT1(8%)、BRCA2(5%)、PTEN(7.5%)和ESR1(3%)等3-5。
临床实践小tips:

看“基因名称”,查找您关注的基因。
2.变异类型
常见的基因突变类型包括:替换、缺失、插入、缺失插入、重复、移码。
表1.变异类型及意义
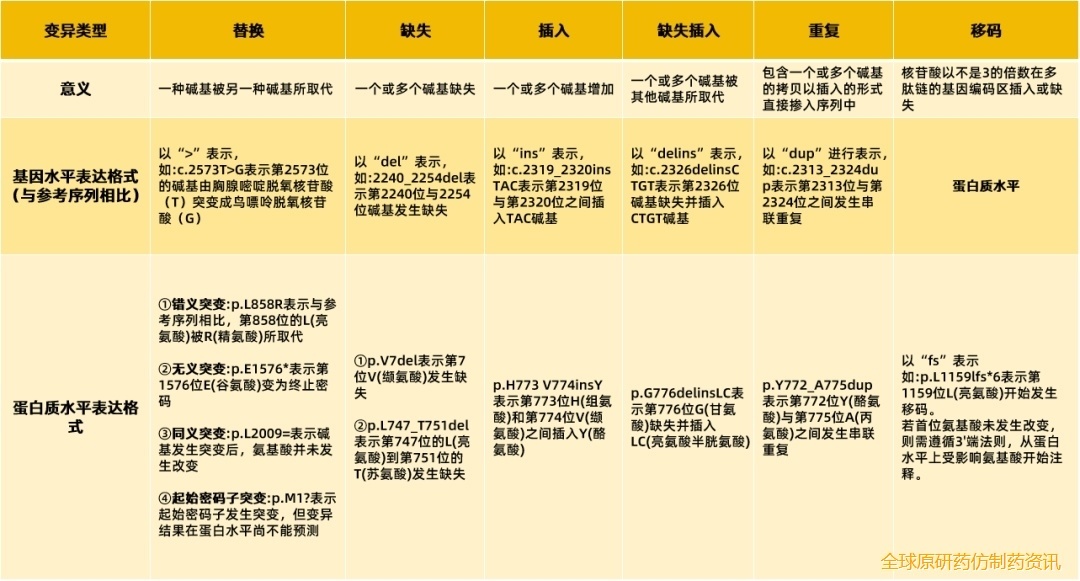
临床实践小tips:

在基因或蛋白质水平发生变化后不一定具有致病性,应结合下文AMP/ASCO/CAP等指南解读。
3.突变丰度/拷贝数
突变丰度指该位点所有等位基因中,突变等位基因的具体占比。以该NGS报告为例,突变丰度11.9%意为该位点含有11.9%的突变等位基因和88.1%的野生型等位基因,送检样本的肿瘤细胞含量是影响基因突变/重排丰度(AF/VAF)高低的重要因素之一。
根据《肿瘤二代测序临床报告解读共识》6,对于组织检测的NGS结果,某基因X的变异AF可通过以下算式计算:
X基因的变异AF=肿瘤细胞占比×肿瘤中X变异的克隆占比×0.5(杂合突变)
以上为变异AF的粗略计算方式,实际上还需要同时考虑拷贝数变异等干扰因素的影响。拷贝数变异结果以发生扩增或缺失后的具体拷贝数(CN)表示,正常情况下,常染色体基因拷贝n=2。当某段DNA发生缺失,则可能只有1个甚至0个拷贝;当发生重复/扩增,就可能出现3个甚至更多拷贝。在癌症中,肿瘤常伴随基因扩增或缺失并表现为拷贝数变化。
临床实践小tips:

NGS并非单细胞测序,其报告中的突变AF/VAF/频率是送检样本的”均值”。
4.突变位点
根据人类基因组变异协会(HGVS)建立的序列变异命名系统将突变内容分为三个部分:转录本、基因水平的脱氧核苷酸改变及蛋白质水平的氨基酸改变。
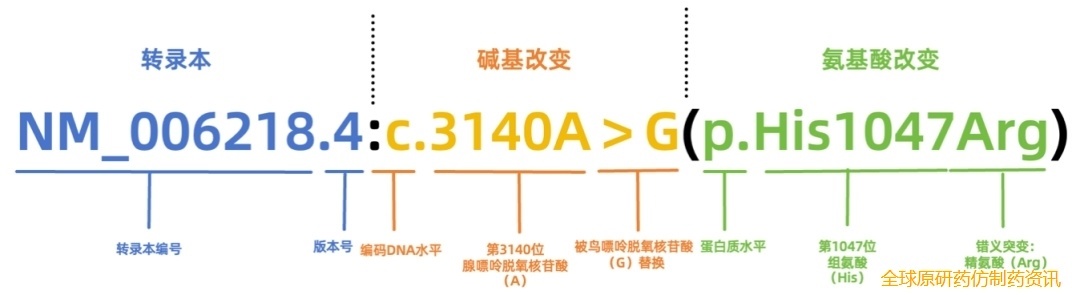
图1.突变位点示意图
临床实践小tips:

同一基因变异在不同基因组版本中的坐标(绝对位置)是不同的。在分析变异及报告时,必须注明参考基因组序列的组装版本号:GRCh37或GRCh38(即hg19或hg38)7。在此基础上,还应在报告或交流变异时,注明RefSeq转录本(基因和转录本参考序列)编号(如NM _006218.4),以确保同一变异经注释后是同样的碱基/氨基酸变异。因此,为促进临床参照的一致性,美国国家生物技术信息中心(NCBI)和欧洲分子生物学实验室-欧洲生物信息学研究所(EMBL-EBI)合作发布参考转录本数据库MANE(Matched Annotation from the NCBI and EMBL-EBI),其中MANE Select集旨在作为临床报告的通用标准,及临床报告的常用转录本编号,供临床、科研交流使用。
5.证据等级
NGS报告的核心价值在于识别“有临床意义的驱动突变”,需结合突变的功能机制、循证等级及临床意义分级,筛选高优先级靶点。应用较广泛的分级标准是在2017年由AMP/ASCO/CAP联合制定的体细胞变异解读指南8,其中将基因变异按照其临床意义的重要性分为Ⅰ-Ⅳ四个等级,依次由高到低:
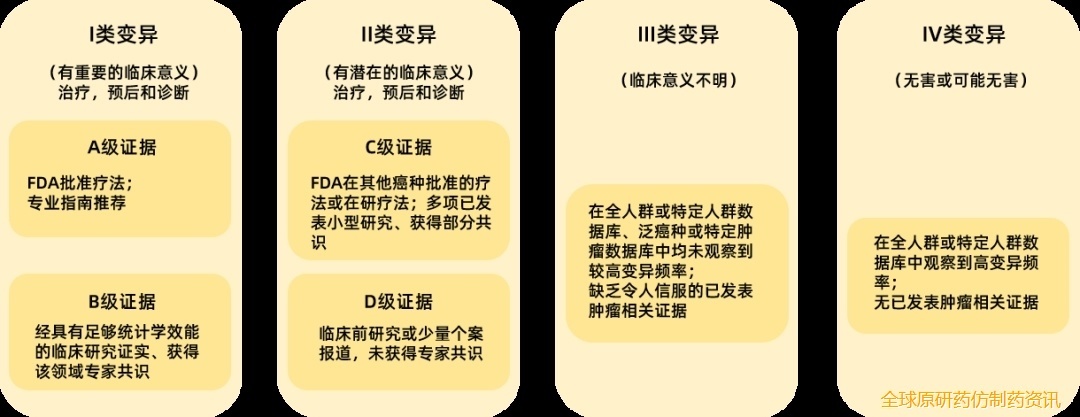
图2.AMP/ASCO/CAP指南:基于证据的体细胞突变分类8
其他循证分级系统还包括分子靶点临床可操作性量表(ESCAT量表)和精准医疗肿瘤数据库(OncoKB)证据等级规则。
表2.ESCAT量表9
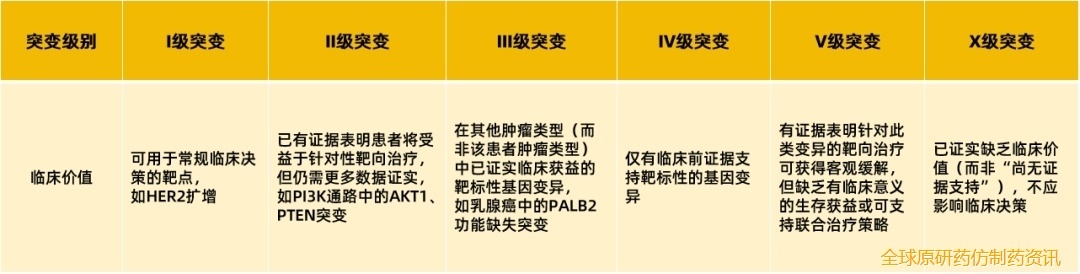
表3.OncoKB证据等级规则10
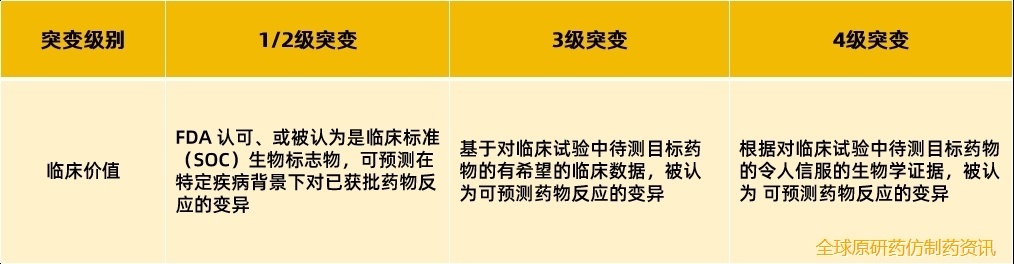
6.靶向药物
能否根据检测结果匹配有效的靶向药,是患者最为关注的问题之一。在检测出具有临床意义的基因突变后,同时确认该份NGS报告质控合格情况下,临床医生可在综合考虑患者情况后首选A类(获FDA批准或专业指南推荐)靶向药物。
临床实践小tips:

临床应根据药物适应证、临床试验入排标准、患者个人意愿等多方面进行治疗方案决策。
7.药物敏感性
部分NGS报告会根据检出的不同驱动基因变异,结合最新药物获批情况、指南与共识,罗列出对应的靶向药物应用敏感性信息。检测结果与药物关系主要分为敏感/正相关和不敏感/负相关。敏感/正相关包括敏感、可能敏感、疗效好、预后好等情况;不敏感/负相关包括耐药、可能耐药、疗效差、预后不好等情况。
一、样本质控
基因检测的质控指标包括肿瘤细胞占比、DNA/RNA提取量、测序深度等,通常与样本质量或测序质量有关。在样本送检前,应在伦理允许范围内向受检者详细说明现有检测技术的局限性,如单基因检测的准确性和检出率等;芯片、多基因测序(MPS)等检测方法的基因解读的限制和不确定性突变基因的情况等11。
临床实践小tips:

样本质控结果可能会直接影响到检测结果的准确性,肿瘤细胞占比不足、平均测序深度不够、覆盖均一性不足等可能导致NGS报告出现假阴性6,而福尔马林固定过程中导致的化学修饰、数据分析中产生序列伪影等可能导致报告出现假阳性12,当检测报告的质控内容出现异常时,应及时联系病理医生或检测机构,积极采取对应措施。
临床实践小tips:

基因检测应当依据相关操作要求对实验室设置、人员培训和样本采集与保存等方面进行严格管理以提升质控结果。对于数据量不够或者平均测序深度不合格的情况,需要进行加测,保证足够数据量产出和测序深度13;针对DNA降解严重的样本可进行修复以提高检出率,但共识一般推荐尽量选择2年内的石蜡包埋样本,以确保检测的成功性和结果的准确性2。对于保存不规范、时间过长的组织样本应谨慎选择,必要时可可采取血液样本或其他体液样本作为补充14。
表4.NGS报告中的样本主要质控参数示例6
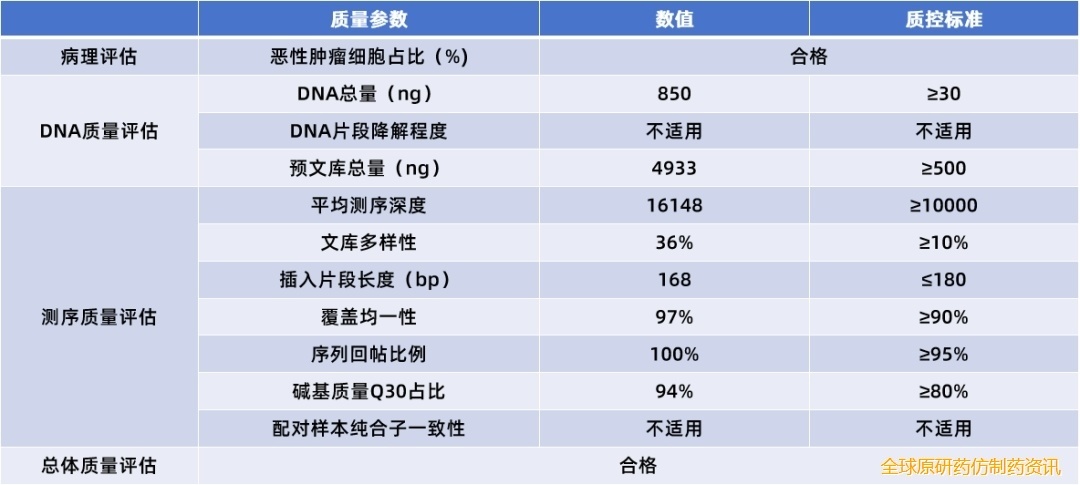
二、“全阴”就是没有基因突变吗?
根据《肿瘤二代测序临床报告解读共识》6,面对未能检出任何肿瘤体细胞突变的报告(即“全阴”报告),需从以下方面溯源,避免错失治疗机会。
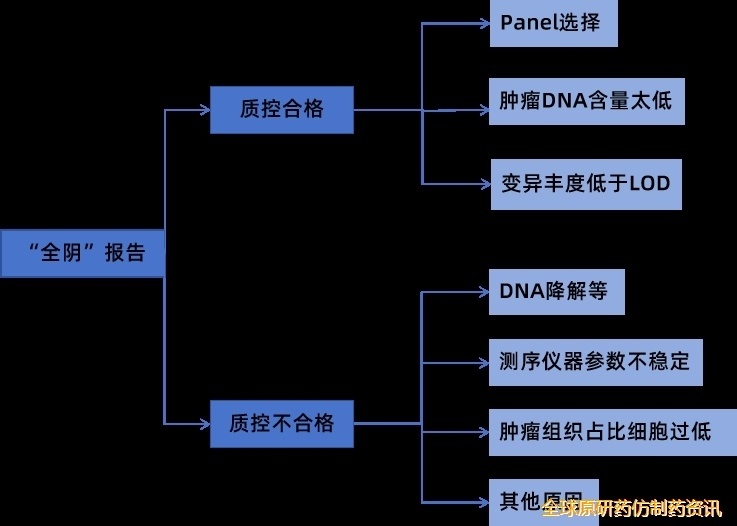
图3.NGS“全阴”报告解读6
(1) 送检样本是肿瘤组织、外周血循环游离DNA(cfDNA)或其他。若为外周血样本,需评估ctDNA浓度是否达标,若ctDNA肿瘤分数≥1%,外周血ctDNA与组织NGS结果一致率为97.1%;若ctDNA肿瘤分数<1%,应进行组织学NGS确认患者基因变异携带状态;若为组织样本,需确认肿瘤细胞占比是否≥20%(可通过病理图像分析等方法确认)6,15-16。结合样本质控信息及患者治疗史(如患者正接受有效的抗肿瘤治疗),综合判断样本中是否含有足够肿瘤成分,是否因以上原因导致DNA总提取量低于NGS的最低检测限(LOD)并及时补送样本。
(2) 选择的NGS panel是否与患者的肿瘤类型相匹配,即该肿瘤所关注的特定变异及启动子突变是否能被该panel覆盖。若选择的NGS panel不匹配,则“全阴”结果可能并不能反映肿瘤基因组变异状态,仅能提示“基因突变状态未知”。
以上评估可以帮助我们判断,该“全阴”结果是提示“X基因野生型”可能性大,还是“X基因状态未知”可能性大。
临床实践小tips:

若一份血检报告提示“全阴”,且已确认panel覆盖区域足够,此时的“全阴”,很可能仅提示肿瘤全身负荷较低或其他原因,如患者正接受有效的抗肿瘤治疗,导致释放入血的ctDNA含量极低、未达检测平台的LOD。这种“全阴”不能反映肿瘤基因组变异状态,仅能提示“基因突变状态未知”,这种血检报告可以提供突变谱以外的其他信息,在特定场景下提示一定的预测、预后价值6。术后患者可等待两周再采集血样中的ctDNA,并建议在一个月后随访采样以确认阴性结果17。
小结
在肿瘤精准治疗中,NGS报告解读需遵循系统化原则,强调质控优先,聚焦突变分级,关注Ⅰ/Ⅱ类变异指导治疗,规避Ⅲ/Ⅳ类变异引发的过度医疗风险。在此基础上,可开展MDT协作,综合患者肝肾功能、药物可及性等因素,综合平衡治疗获益与安全性。临床实践中,需将临床证据与患者个体特征深度整合,方能实现NGS报告驱动的精准医疗,切实提升患者生存质量。
专家简历
欧阳能太 教授
中山大学孙逸仙纪念医院细胞分子诊断中心教授
中国医学装备协会基因检测分会常委
中国抗癌协会肿瘤基因诊断专委会常委
中国抗癌协会肿瘤标志专委会常委
中华医学会病理学分会分子病理学组委员
广东省精准医学应用学会临床生物信息分会主任委员
广东省基层医药学会细胞病理与分子诊断专委会主任委员
广东省抗癌协会肿瘤标志专委会副主任委员
广东省基层医药学会精准医学专委会副主委
广东省精准医学应用学会病理技术分会名誉主任委员
广东省精准医学应用学会分子病理分会副主任委员
广东省医学教育协会生殖与遗传管理专委会副主任委员
广东省保健协会甲状腺保健分会副主委
审批编号:CN-178765
有效期至:2027-02-11
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
编辑:Luna/Uni
审校:欧阳能太教授
排版:Chipsy
执行:Squid
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
生成海报
 长按扫码关注公众号
长按扫码关注公众号