
2025年9月15日发表于
Therapeutic Advances in Medical Oncology
摘要
小细胞肺癌(SCLC)是一种侵袭性很强的癌症,大多数病例在确诊时已处于广泛期(ES-SCLC)。铂类和依托泊苷化疗是目前一线治疗的主要方案,初始缓解率较高。然而,耐药性发展迅速,导致总体生存期较差,后续治疗效果有限,尤其对于铂类耐药患者。在ES-SCLC的一线化疗中加入免疫检查点抑制剂(ICIs)可略微改善生存期。对于接受根治性放化疗的局限期小细胞肺癌(LS-SCLC),ICI度伐利尤单抗已被批准作为巩固治疗,以降低复发风险。目前正在开展更多临床试验,研究ICIs与放化疗联合应用,以及作为巩固或维持治疗的疗效。对于复发性小细胞肺癌,治疗方案包括拓扑替康或鲁比替定等化疗药物,以及卡铂/依托泊苷再次治疗。靶向δ样配体3的双特异性T细胞衔接器(BiTE)tarlatamab/塔拉妥单抗已获FDA批准用于治疗铂类化疗后疾病进展的广泛期小细胞肺癌(ES-SCLC),目前正在评估其在更早期治疗中的应用。其他BiTE也处于早期研发阶段,并展现出令人鼓舞的早期活性。包括sacituzumab govitecan在内的多种抗体药物偶联物正在进行临床试验,并已显示出令人鼓舞的疗效。旨在克服化疗和免疫疗法耐药性的新型靶向疗法也处于临床前研发阶段。尽管取得了这些进展,但由于缺乏用于预测治疗结果的有效生物标志物,进展仍然受到阻碍。识别具有不同治疗脆弱性的SCLC转录亚型为更好地进行治疗分层带来了希望。SCLC-I转录亚型、肿瘤突变负荷和肿瘤免疫细胞特征是预测免疫检查点抑制剂(ICI)长期生存获益的潜在生物标志物。循环肿瘤DNA和循环肿瘤细胞已展现出在预后判断、分子分型和肿瘤监测方面的潜力。然而,仍需开展进一步研究,以支持治疗分层、延长治疗反应、克服耐药性并最终改善这种致命疾病的治疗效果。
介绍
小细胞肺癌(SCLC)是一种高级别神经内分泌癌,约占所有肺癌的15%。其特征是快速增殖和早期转移。约三分之一的患者被诊断为局限期小细胞肺癌(LS-SCLC),此时癌细胞尚未扩散至一侧胸腔或区域淋巴结以外,此类患者可以接受根治性治疗。其余三分之二的患者就诊时已处于广泛期小细胞肺癌(ES-SCLC),此时癌细胞已扩散至一侧胸腔或区域淋巴结以外。对于广泛期小细胞肺癌,姑息性全身治疗±巩固性放疗是唯一的治疗选择。小细胞肺癌预后不良,局限期小细胞肺癌的中位总生存期(mOS)不足2.5年,广泛期小细胞肺癌的中位总生存期不足1年。
尽管小细胞肺癌(SCLC)初期对治疗高度敏感,但大多数病例会迅速产生耐药性,导致缓解持续时间短、复发率高,且后续治疗效果不佳。SCLC具有高频率的体细胞突变和相应的高肿瘤突变负荷(TMB),以及显著的肿瘤间和肿瘤内异质性,且化疗后异质性进一步增加。这些特征,以及表型可塑性,共同促成了SCLC的侵袭性和耐药性的产生。大多数SCLC肿瘤携带抑癌基因TP53和RB1的失活突变。约25%的病例中观察到MYC家族癌基因扩增。其他一些较少发生改变的基因与细胞周期调控和细胞凋亡(例如TP73、RBL1、RBL2)、NOTCH信号通路(例如NOTCH1-4)、表观遗传修饰(例如CREBBP、EP300、KMT2A-D)、细胞骨架和黏附调控(例如ALMS1、ASPM、COL22A1)以及激酶信号通路(例如PIK3CA、PTEN)相关。小细胞肺癌(SCLC)肿瘤通常表现出神经内分泌表型,其中一小部分表现出非神经内分泌特征。虽然突变谱分析目前尚未识别出广泛的亚型,但转录谱分析已根据神经源性转录因子的差异表达识别出不同的亚型。神经内分泌亚型包括ASCL1(SCLC-A)、NEUROD1(SCLC-N)和ATOH1,而POU2F3(SCLC-P)则代表非神经内分泌表型。近期发现的一种“炎症型”亚型(SCLC-I)的特征是ASCL1、NEUROD1和POU2F3表达低,同时免疫检查点基因和其他免疫相关基因的表达水平升高。Delta样配体3 (DLL3) 是一种抑制性NOTCH配体,在神经内分泌型小细胞肺癌 (SCLC) 细胞表面异常表达,尤其是在ASCL1驱动的亚型中,但在正常组织中基本不表达。这种肿瘤特异性表达使DLL3成为SCLC中一个有前景的生物标志物和治疗靶点。
尽管人们对小细胞肺癌(SCLC)的异质性有了更深入的了解,但目前尚无已验证的生物标志物可用于指导治疗选择或精准医疗。这凸显了开发更有效的治疗方法、改进生物标志物导向的治疗策略以及个体化治疗以改善临床疗效和总生存期(OS)的迫切需求。本综述重点关注2018年至2024年间发表的SCLC II期和III期临床试验,以及早期的关键性研究,并纳入重要的I期和正在进行的试验,以突出新兴的治疗方法。本综述总结了当前关于标准治疗方案、临床试验中的新型疗法、新兴治疗靶点以及用于治疗选择的预后和预测性生物标志物的证据。
目前小细胞肺癌的治疗方法
局限期小细胞肺癌的一线治疗
小细胞肺癌(SCLC)的治疗根据局限期(LS-SCLC)和广泛期(ES-SCLC)进行分层。对于极早期局限期小细胞肺癌(T1-2N0M0),可考虑手术切除,术后辅助铂类/依托泊苷化疗。一项回顾性研究表明,对于切除的pT1-2N0M0期肿瘤,辅助化疗±放疗较未接受辅助治疗的患者具有更长的中位总生存期(mOS)(66.0个月 vs 42.0个月,p<0.01)。在一项纳入507例I/II期患者的回顾性研究中,接受肺叶切除术和辅助化疗(淋巴结阳性时包括放疗)的患者较仅接受同步放化疗的患者具有更长的中位总生存期(48.6个月 vs 28.7个月,p<0.0001)。然而,决定进行手术而不是放化疗,必须权衡等待期间病情进展的风险,这可能取决于治疗中心的资源和能力。
对于大多数不适合或不建议手术的局限期小细胞肺癌(LS-SCLC)病例,通常采用以治愈为目的的化疗和胸部放疗。同步放化疗通常包括顺铂/依托泊苷化疗,并在第二个化疗周期同时进行胸部放疗,每日两次。根据CONVERT试验,该方案的中位无进展生存期(mPFS)为15.4个月,中位总生存期(mOS)为30.0个月。对于无法接受同步放化疗的患者,序贯放化疗是一种替代方案,但其生存期较短。日本一项III期临床试验报告显示,接受序贯放化疗的局限期小细胞肺癌患者的中位总生存期为19.7个月,而接受同步放化疗的患者中位总生存期为27.2个月。如果存在禁忌症或毒性方面的担忧,卡铂可作为顺铂的替代方案。一项针对接受同步或序贯放化疗的局限期小细胞肺癌(LS-SCLC)患者的回顾性研究表明,与卡铂相比,顺铂可略微改善总生存期(OS)和局部区域控制率,但差异无统计学意义。III期CONVERT试验显示,从LS-SCLC治疗的第2个疗程开始,接受每日一次放疗与每日两次放疗的LS-SCLC患者的中位总生存期(mOS)无显著差异(30个月 vs 25个月,p=0.14)。然而,由于该试验旨在证明每日一次放疗的优效性而非等效性,因此每日两次放疗仍然是标准治疗方案。
尽管采用了根治性放化疗,局限期小细胞肺癌(LS-SCLC)的复发率仍然很高,约70%的患者会在5年内复发。这凸显了开发其他治疗方法以降低复发风险和提高生存率的必要性。程序性死亡配体1(PD-L1)免疫检查点抑制剂(ICI)度伐利尤单抗(durvalumab)近期已获批用于放化疗后的治疗。ADRIATIC III期临床试验表明,接受同步放化疗后无疾病进展的局限期小细胞肺癌(LS-SCLC)患者,若接受度伐利尤单抗巩固治疗长达24个月,其中位无进展生存期(mPFS)(16.6个月 vs 9.2个月,p=0.02)和中位总生存期(mOS)(55.9个月 vs 33.4个月,p=0.01)均显著长于安慰剂组,最终促成了度伐利尤单抗于2024年12月获得FDA批准上市。目前正在等待第三组接受度伐利尤单抗联合细胞毒性T淋巴细胞相关蛋白(CTLA-4)抑制剂曲美利单抗巩固治疗的患者的结果。ADRIATIC试验的局限性包括缺乏生物标志物评估(例如PD-L1)以指导未来的治疗分层。研究者可酌情决定是否给予预防性颅内放疗(PCI)(两组均为54%),但PCI组和非PCI组的总生存期(OS)无显著差异。度伐利尤单抗组和安慰剂组的3-4级毒性反应相似,但长期毒性数据尚待公布。相比之下,NRG-LU005试验结果显示,接受阿特珠单抗同步放化疗后,接受阿特珠单抗巩固治疗长达1年的局限期小细胞肺癌(LS-SCLC)患者,与单纯放化疗相比,中位无进展生存期(mPFS)(11.5个月 vs 12.0个月,风险比(HR)=1.00,95%置信区间(CI)0.80-1.25)或中位总生存期(mOS)(39.5个月 vs 33.1个月;HR=1.11,95% CI 0.85-1.45)均无显著差异。然而,与ADRIATIC研究不同,NRG-LU005研究仅纳入接受一个疗程化疗的患者,且未要求在放化疗后确认疾病控制情况,这表明对于局限期小细胞肺癌 (LS-SCLC) 患者,一线同步免疫检查点抑制剂 (ICI) 治疗可能并非最佳方案。目前正在进行的临床试验正在评估其他ICI治疗LS-SCLC的疗效,包括一线联合放化疗以及作为巩固或维持治疗(表1)。III期DeLLphi-306试验正在研究靶向DLL3的BiTE tarlatamab与安慰剂在同步放化疗后的疗效比较 (NCT06117774)。
表1. ICIs与放化疗联合治疗LS-SCLC的临床试验。
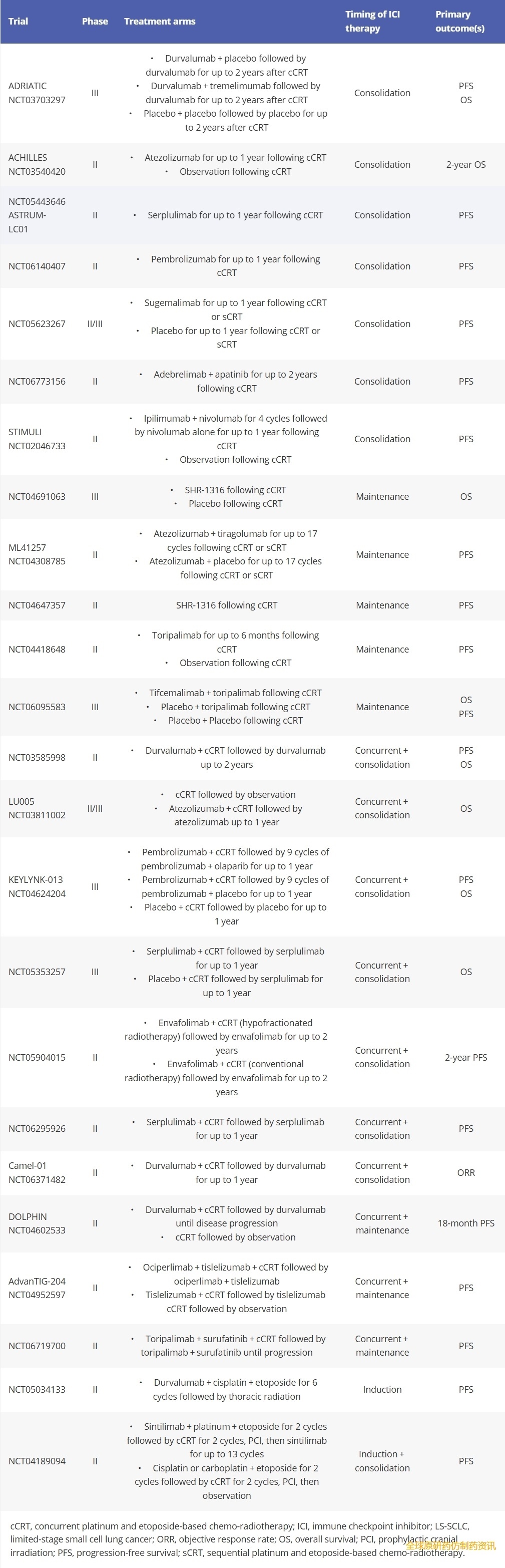
广泛期小细胞肺癌的一线治疗
铂类/依托泊苷化疗是广泛期小细胞肺癌(ES-SCLC)一线治疗的基石。一项包含36项临床试验的荟萃分析比较了不同的化疗方案,发现含顺铂和/或依托泊苷的方案可显著提高生存率。由于卡铂与顺铂的缓解率相似,但毒性更低,因此通常优先选择卡铂。铂类/依托泊苷化疗通常进行4至6个疗程,之后进行监测,因为研究表明维持化疗并未显著改善总生存期(OS)。伊立替康和吉西他滨与卡铂联合使用时,疗效和预后与依托泊苷相似。
近期临床试验探索了免疫检查点抑制剂(ICIs)与铂类/依托泊苷化疗联合应用(表2)。根据IMPower133和CASPIAN试验的结果,PD-L1抑制剂阿特珠单抗或度伐利尤单抗分别被推荐与铂类/依托泊苷联合用于一线治疗。在III期IMPower133试验中,接受阿特珠单抗联合卡铂/依托泊苷一线治疗,随后接受阿特珠单抗维持治疗的广泛期小细胞肺癌( ES-SCLC)患者的中位总生存期(mOS)显著长于接受安慰剂联合卡铂/依托泊苷治疗的患者(12.3个月 vs 10.3个月,p=0.0154)。同样,在CASPIAN III期试验中,接受度伐利尤单抗联合铂类/依托泊苷治疗,随后接受度伐利尤单抗维持治疗的广泛期小细胞肺癌 (ES-SCLC) 患者的中位总生存期 (mOS) 长于仅接受铂类/依托泊苷治疗的患者(13.0 个月 vs 10.3 个月,p=0.0047)。IMpower133试验的局限性在于它没有纳入PD-L1或TMB等生物标志物分析。虽然CASPIAN试验纳入了生物标志物分析,但该分析属于探索性分析,且受限于数据不完整(约54%的患者样本可用于PD-L1评估,约 33% 的患者样本可用于组织TMB评估)、各治疗组间样本可用性不平衡以及缺乏基于血液的TMB评估。此外,这两项试验均未纳入巩固性胸部放疗,而巩固性胸部放疗是ES-SCLC单纯化疗治疗的公认组成部分。此外,免疫检查点抑制剂 (ICI) 的绝对生存获益也较为有限。在IMPower133研究中,阿特珠单抗/卡铂/依托泊苷组的18个月总生存率为34.0%,而卡铂/依托泊苷组为21.0%,表明仅有13.0%的患者获得了长期总生存获益。同样,在CASPIAN研究中,度伐利尤单抗/卡铂/依托泊苷组的3年总生存率为17.6%,而卡铂/依托泊苷组为5.8%,表明仅有11.8%的患者获得了长期总生存获益。这些结果引发了人们对未经筛选的患者长期获益和成本效益的担忧,并凸显了预测性生物标志物在筛选最有可能从免疫检查点抑制剂(ICIs)治疗中获益的患者方面的必要性。
表2.免疫检查点抑制剂联合铂类/依托泊苷化疗一线治疗ES-SCLC的关键临床试验。
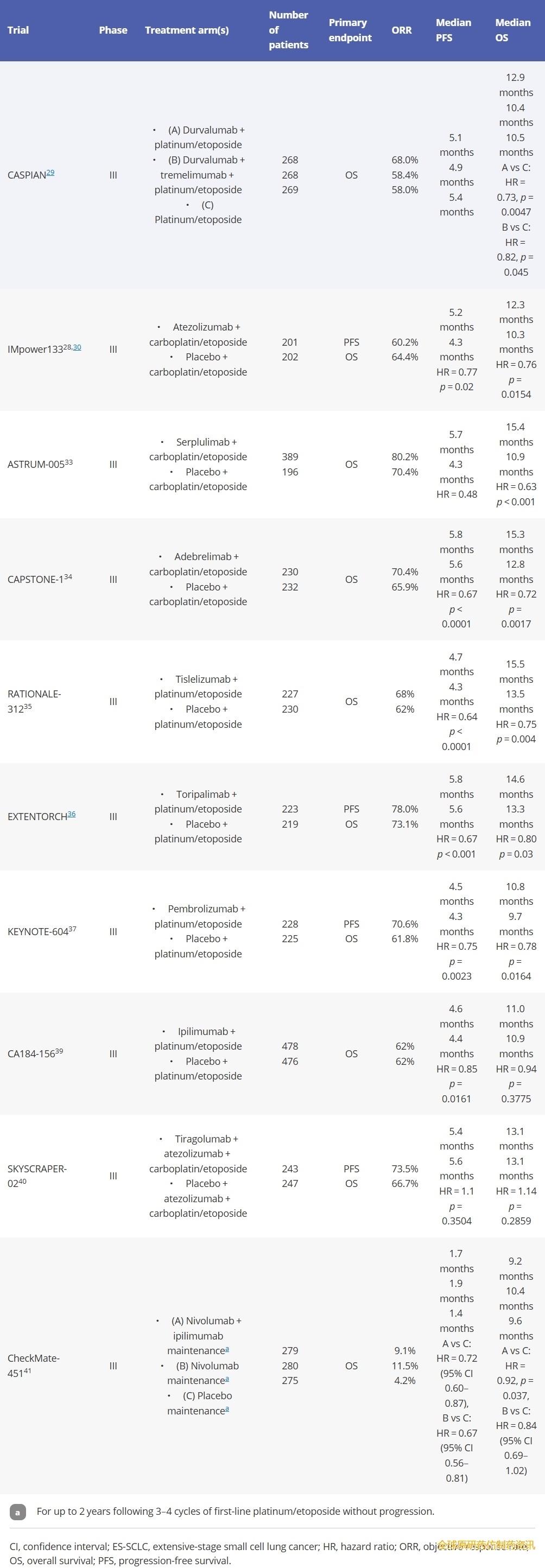
程序性死亡蛋白1 (PD-1) 抑制剂也已与化疗联合应用进行研究。在III期ASTRUM-005试验中,接受卡铂/依托泊苷联合serplulimab治疗后序贯serplulimab维持治疗的广泛期小细胞肺癌 (ES-SCLC) 患者的中位总生存期 (mOS) 显著长于接受卡铂/依托泊苷联合安慰剂治疗的患者(15.4个月 vs 10.9个月,p<0.001)。因此,serplulimab成为首个获批与化疗联合用于治疗ES-SCLC的PD-1抑制剂。
在中国开展的三项针对广泛期小细胞肺癌(ES-SCLC)患者的III期临床试验也证实了PD-L1/PD-1抑制剂可改善患者预后。在III期CAPSTONE-1试验中,接受阿德布雷利单抗(抗PD-L1)联合卡铂/依托泊苷治疗,随后接受阿德布雷利单抗维持治疗的患者,其中位总生存期(mOS)较接受安慰剂联合卡铂/依托泊苷治疗的患者更长(15.3个月 vs 12.8个月,p=0.0017)。在III期RATIONALE-312试验中,接受替雷利珠单抗(抗PD-1)联合铂类/依托泊苷治疗,随后接受替雷利珠单抗维持治疗的患者,其中位总生存期(mOS)较接受安慰剂联合铂类/依托泊苷治疗的患者更长(15.5个月 vs 13.5个月,p=0.004)。最后,在III期EXTENTORCH试验中,接受特瑞普利单抗(抗PD-1)联合铂类/依托泊苷治疗,随后接受长达2年特瑞普利单抗维持治疗的广泛期小细胞肺癌 (ES-SCLC) 患者,其中位总生存期 (mOS) 长于接受安慰剂联合铂类/依托泊苷治疗的患者(14.6个月 vs 13.3个月,p=0.03)。
其他免疫检查点抑制剂(ICIs)的临床试验大多结果为阴性。在III期KEYNOTE-604试验中,PD-1抑制剂帕博利珠单抗联合铂类/依托泊苷治疗组的中位总生存期(mOS)较单用铂类/依托泊苷治疗组有所改善,但未达到统计学意义(10.8个月 vs 9.7个月,p=0.0164)。伊匹木单抗在II期试验中与铂类/依托泊苷一线治疗组联合应用,但未见mOS较单用铂类/依托泊苷治疗组有所改善。TIGIT抑制剂替拉戈利单抗在SKYSCRAPER-02 II期试验中与卡铂/依托泊苷联合应用,但未见mPFS或mOS的改善。此外,免疫检查点抑制剂也曾被研究作为维持治疗方案。CheckMate-451 III期临床试验表明,对于接受最多4个周期铂类/依托泊苷化疗的广泛期小细胞肺癌(ES-SCLC)患者,维持治疗期间,使用伊匹木单抗(抗CTLA-4)联合纳武利尤单抗(抗PD-1)或单用纳武利尤单抗,疗程长达2年,与安慰剂相比,并未改善中位总生存期(mOS)。迄今为止,免疫检查点抑制剂(ICI)联合化疗尚未显示出优于单药ICI的疗效;在CASPIAN试验中,在度伐利尤单抗/铂类/依托泊苷方案中加入CTLA-4抑制剂曲美木单抗也未改善mOS。
III期IMforte试验研究了在接受4个周期卡铂/依托泊苷化疗后未出现疾病进展的广泛期小细胞肺癌(ES-SCLC)患者中,在维持治疗方案中加入鲁比奈替定(lurbinectedin)的疗效。42例患者被随机分配接受阿特珠单抗维持治疗,或同时接受鲁比奈替定治疗,直至疾病进展。与单用阿特珠单抗相比,鲁比奈替定联合阿特珠单抗维持治疗组的中位无进展生存期(mPFS)更长(5.4个月 vs 2.1个月,p<0.0001),中位总生存期(mOS)也更长(13.2个月 vs 10.6个月,p=0.017),均从维持治疗开始计算。联合治疗组3-4级不良事件发生率更高(38% vs 22%),主要由血液学毒性引起。接受过巩固性胸部放疗的患者被排除在外。这些研究结果支持lurbinectedin联合atezolizumab作为ES-SCLC的一种有前景的维持治疗策略,尽管在合并症较多的患者群体中的耐受性以及巩固性胸部放射治疗的作用仍有待评估。
在化疗中加入抗PD-L1/PD-1免疫检查点抑制剂(ICIs)仅能带来有限的生存获益,而其他类型ICIs则缺乏疗效,这凸显了寻找更有效策略来克服免疫逃逸和ICIs耐药性的必要性。生物标志物指导的分层对于识别最有可能从免疫治疗中获益的患者也至关重要。小细胞肺癌(SCLC)中的几种免疫逃逸机制可能成为治疗靶点。尽管SCLC具有较高的肿瘤突变负荷(TMB),但由于抗原呈递缺陷,其免疫原性较低,这部分是由于主要组织相容性复合体(MHC)I类分子表达缺陷限制了CD8+T细胞的识别,以及MHC II类分子表达降低损害了CD4+T细胞的活化。SCLC肿瘤通常也表现为“免疫冷”,肿瘤浸润淋巴细胞(TILs)水平较低,尤其是CD8+T细胞。肿瘤细胞和基质细胞分泌的血管内皮生长因子(VEGF)也会破坏免疫细胞的黏附和迁移,这为将VEGF抑制剂与免疫检查点抑制剂(ICIs)联合使用提供了理论依据。小细胞肺癌(SCLC)细胞产生的肿瘤浸润淋巴细胞(TIL)募集所需的趋化因子水平也较低。由于NKG2DL等NK激活配体的表达降低和表观遗传沉默,自然杀伤(NK)细胞介导的固有免疫反应受损。此外,肿瘤微环境富含免疫抑制细胞,包括调节性T细胞、肿瘤相关巨噬细胞、髓源性抑制细胞和癌相关成纤维细胞,所有这些细胞都有助于抑制抗肿瘤免疫反应。恢复抗原呈递、促进免疫细胞浸润和/或逆转免疫抑制的疗法可以增强现有免疫检查点抑制剂的疗效,并指导小细胞肺癌新型免疫疗法的开发。
巩固性胸部放疗在广泛期小细胞肺癌中的作用
对于接受铂类化疗后获得缓解的广泛期小细胞肺癌(ES-SCLC)患者,通常会进行巩固性胸部放疗。在一项前瞻性研究中,210例接受一线顺铂/依托泊苷治疗(3个周期)的患者中,局部至少达到部分缓解且远处转移达到完全缓解的患者被随机分配至接受卡铂/依托泊苷联合胸部放疗或继续接受4个周期顺铂/依托泊苷治疗。其中52例远处转移达到完全缓解的患者还接受了预防性胸腔镜手术(PCI)。接受胸部放疗的患者的中位总生存期(mOS)长于未接受放疗的患者(17个月 vs 11个月,p=0.041)。在针对一线铂类/依托泊苷治疗后获得缓解并接受PCI的ES-SCLC患者的III期CREST试验中,接受胸部放疗的患者的6个月无进展生存期(PFS)为24%,而未接受胸部放疗的患者为7%(p=0.001)。尽管1年总生存率(OS)无显著差异,但胸部放疗组的2年OS更高(13% vs 3%,p=0.004)。化疗后存在胸内残留病灶的患者,接受胸部放疗后中位无进展生存期(mPFS)和中位总生存期(mOS)均更佳,但对于无残留病灶的患者,两组间无显著差异。目前尚不确定接受一线PD-(L)1抑制剂联合化疗,随后进行维持治疗的患者,能否从巩固性胸部放疗中获益。一项包含15项回顾性研究的荟萃分析显示,接受一线化疗联合免疫治疗,随后进行巩固性胸部放疗的广泛期小细胞肺癌(ES-SCLC)患者的生存率高于未接受胸部放疗的患者。目前正在前瞻性临床研究中对此进行探讨。
PCI在小细胞肺癌一线治疗中的作用
由于脑转移复发风险高,预防性脑照射(PCI)通常用于一线治疗有效的局限期小细胞肺癌(LS-SCLC)患者和年龄小于70岁的广泛期小细胞肺癌(ES-SCLC)患者。然而,降低脑转移风险的同时,也应权衡慢性神经毒性的风险。一项纳入7项临床试验的荟萃分析显示,对于一线治疗后达到完全缓解的LS-SCLC或ES-SCLC患者,PCI可使3年累积脑转移发生率降低25.3%,3年生存率提高5.4%。近期一项纳入223项LS-SCLC或ES-SCLC患者研究的荟萃分析表明,与未接受PCI的患者相比,接受PCI的患者总生存期(OS)更长(HR=0.59,p<0.001)。在63项研究中,接受PCI治疗的患者脑转移发生率较低(相对风险,0.45,p<0.001)。然而,在对9项研究进行事后分析时,这些患者在接受一线治疗结束后均接受了MRI检查以排除脑转移,结果显示,接受PCI治疗的患者与未接受PCI治疗的患者的中位总生存期(mOS)无显著差异(HR=0.74,p=0.08),这表明PCI在改善总生存期方面可能并不优于监测。
在一项针对化疗有效的广泛期小细胞肺癌(ES-SCLC)患者的III期临床试验中,接受预防性脑照射(PCI)的患者发生症状性脑转移的风险较低(HR=0.27,p<0.001),且1年累积脑转移风险也较低(14.6% vs 40.4%)。PCI还与更长的中位总生存期(mOS)相关(6.7个月 vs 5.4个月,p=0.003)。然而,该研究未纳入入组前的基线脑部影像学检查以确认无脑转移。在另一项III期临床试验中,对铂类化疗有效且入组前脑部MRI未见转移的ES-SCLC患者被随机分配至PCI组或观察组,并接受长达24个月的MRI扫描。PCI组和观察组的mOS无显著差异(11.6个月 vs 13.7个月,p=0.094)。
需要开展更多前瞻性研究,以确定预防性磁共振成像(PCI)在改善总生存期(OS)方面是否优于常规监测,并评估神经毒性的影响,尤其是在标准一线治疗中加入PD-(L)-1抑制剂的情况下。PRIMALung(EORTC-1901)是一项前瞻性随机试验,旨在比较每3个月进行一次磁共振成像(MRI)监测与PCI在OS方面的非劣效性,研究对象为对一线治疗有反应的局限期小细胞肺癌(LS-SCLC)和广泛期小细胞肺癌(ES-SCLC)患者。
转化型小细胞肺癌的治疗
非小细胞肺癌 (NSCLC) 向小细胞肺癌 (SCLC) 的组织学转化是一种日益受到重视的靶向治疗获得性耐药机制,最常见于EGFR突变型腺癌。在接受EGFR酪氨酸激酶抑制剂 (TKI) 治疗的EGFR突变型NSCLC患者中,3%–14%观察到了转化。虽然转化的确切分子机制尚不清楚,但谱系可塑性——以表型从上皮状态向神经内分泌状态转换为特征——被认为是主要驱动因素。肿瘤异质性也可能有所贡献,因为一些肿瘤表现出NSCLC和SCLC的混合组织学特征,提示在TKI治疗的选择压力下,预先存在的SCLC亚克隆发生了扩增。大多数转化肿瘤保留了其原有的EGFR激活突变,并且常伴有TP53和RB1的失活突变,这些突变是原发性小细胞肺癌的典型特征。虽然转化最常见于EGFR突变病例,但也报道在接受TKI治疗以及ICI治疗的ALK或ROS1融合的非小细胞肺癌中发生转化。
目前尚无针对转化型小细胞肺癌(SCLC)的正式临床指南,治疗决策通常参考原发性SCLC的治疗经验。一项回顾性多中心研究显示,53例接受铂类/依托泊苷化疗的患者中,客观缓解率(ORR)为54%,中位无进展生存期(mPFS)为3.4个月。70例转化后接受中位数为两线治疗的患者,接受紫杉烷类药物治疗后,ORR为50%。17例接受单药PD-1抑制剂或伊匹木单抗/纳武利尤单抗联合治疗的患者均未出现疗效,表明免疫检查点抑制剂(ICI)对这类患者无效。基于这些研究结果,铂类/依托泊苷和紫杉烷类药物均被认为是转化型SCLC患者的潜在有效治疗方案。
鉴于转化型小细胞肺癌(SCLC)的预后较原发性SCLC差,且对免疫检查点抑制剂(ICI)耐药,目前正在探索针对性治疗策略。一项II期临床试验(NCT04538378)正在评估度伐利尤单抗联合奥拉帕尼治疗EGFR突变型非小细胞肺癌(NSCLC)并已转化为SCLC的患者的疗效。一项I期临床试验(NCT03567642)正在研究奥希替尼联合铂类/依托泊苷能否预防EGFR/TP53/RB1突变型NSCLC的转化。需要开展更大规模的队列研究,以阐明转化和耐药机制,识别高危患者,更早地发现转化,并指导针对该亚组患者的专项临床试验的开展。
小细胞肺癌的二线及后续治疗
在以铂类药物为基础的一线化疗期间或治疗后90天内进展的小细胞肺癌(SCLC)被认为是铂耐药的,而一线铂类化疗结束后90天或更长时间后复发的SCLC被认为是铂敏感的。一项荟萃分析显示,与铂耐药SCLC患者相比,铂敏感SCLC患者对二线治疗的客观缓解率(ORR)更高(27.7% vs 14.8%,p=0.0001)。因此,对于铂耐药SCLC患者,通常建议其参与临床试验或接受最佳支持治疗(BSC)。
二线及后续化疗方案中,拓扑替康、鲁比替定、环磷酰胺/多柔比星/长春新碱(CAV)方案和脂质体伊立替康等药物已显示出对总生存期(OS)有一定程度的改善。表3总结 了评估复发性小细胞肺癌(SCLC)化疗药物疗效的关键临床试验结果。在一项针对完成一线化疗后60天以上复发的SCLC患者的随机试验中,静脉注射拓扑替康的中位总生存期(mOS)与CAV方案相似(25.0周 vs 25.7周,p=0.795)。然而,与接受CAV治疗的患者相比,接受静脉注射拓扑替康治疗的患者中症状改善的比例更高,尤其是在以下方面:呼吸困难(27.9% vs 6.6%,p=0.002)、厌食(32.1% vs 15.8%,p=0.042)、声音嘶哑(32.5% vs 13.2%,p=0.043)、疲乏(22.9% vs 9.2%,p=0.032)以及日常生活受到影响(26.9% vs 11.1%,p=0.023)。一项针对复发性小细胞肺癌患者的III期临床试验研究了口服拓扑替康,结果显示,与单独使用最佳支持治疗(BSC)相比,联合BSC可延长中位总生存期(25.9周 vs 13.9周)。接受拓扑替康治疗的患者生活质量下降速度也较慢,症状控制效果更佳。在铂敏感小细胞肺癌(SCLC)患者的一项III期临床试验中,口服和静脉注射拓扑替康作为二线治疗方案,显示出相似的疗效和中位总生存期(mOS)。在一项名为RESILIENT的III期临床试验中,研究人员对脂质体伊立替康在铂耐药或铂敏感SCLC患者中的疗效进行了评估,这些患者均在接受一线铂类化疗后出现疾病进展。接受脂质体伊立替康或静脉注射拓扑替康治疗的患者的mOS相似(7.9个月 vs 8.3个月,p=0.3094),但脂质体伊立替康的客观缓解率(ORR)更高(44.1% vs 21.6%,p<0.0001),且≥3级毒性反应发生率更低(42.0% vs 83.4%)。
表3. 复发性小细胞肺癌化疗和免疫检查点抑制剂治疗的关键临床试验。
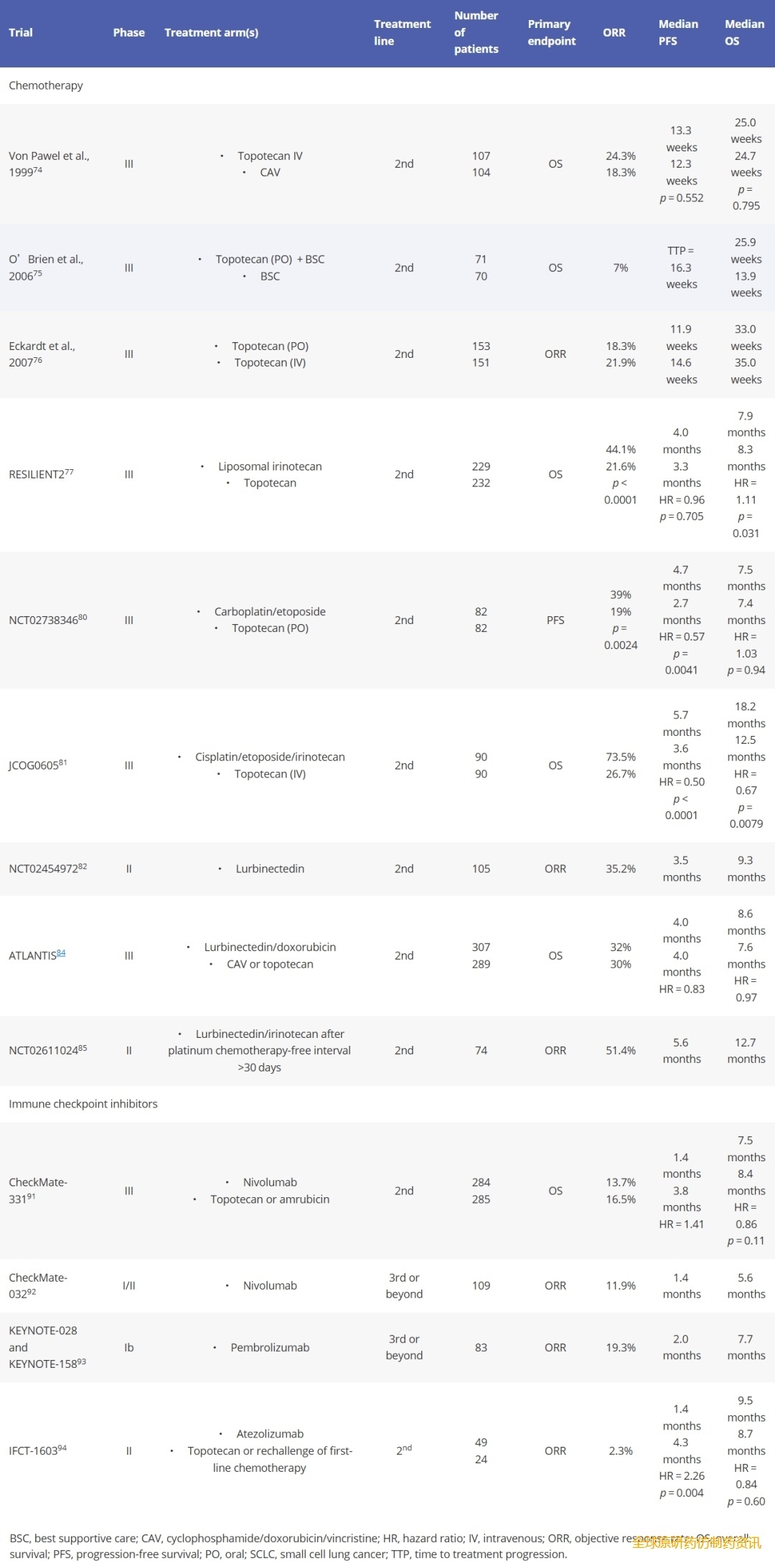
对于铂敏感小细胞肺癌(SCLC)患者,再次使用卡铂/依托泊苷治疗是一个不错的选择。一项纳入112例患者的多中心回顾性研究显示,一线铂类化疗后无治疗间隔期超过90天的患者,接受二线铂类/依托泊苷治疗的客观缓解率(ORR)为45%,中位无进展生存期(mPFS)和中位总生存期(mOS)分别为5.5个月和7.9个月。亚组分析比较了三个无复发生存期(90-119天、120-149天和>150天),结果显示mPFS无显著差异。一项近期纳入93例铂敏感SCLC患者的回顾性多中心研究显示,一线化疗联合免疫治疗后再次接受卡铂/依托泊苷治疗的患者也取得了类似的结果:ORR为59.1%,mPFS为5个月,mOS为7个月。在法国进行的一项 III 期临床试验中,对铂敏感小细胞肺癌患者进行二线再治疗,采用6个疗程的卡铂/依托泊苷方案,其中位无进展生存期(mPFS)显著长于6个疗程的口服拓扑替康方案(4.7个月 vs 2.7个月,p=0.0041)。在JCOG0605 III期临床试验中,研究人员比较了顺铂/依托泊苷/伊立替康三联化疗与静脉注射拓扑替康治疗铂敏感复发性小细胞肺癌患者的疗效。联合化疗组的中位总生存期(mOS)更长(18.2个月 vs 12.5个月,p=0.0079),但超过85%的患者出现3-4级毒性反应,这意味着该方案在临床实践中并不常用。
鲁比替定(Lurbinectedin)是一种转录抑制剂,是复发性小细胞肺癌(SCLC)的一种新型二线治疗方案。在一项II期临床试验中,对于既往接受过化疗且无脑转移的铂耐药或铂敏感SCLC患者,鲁比替定的客观缓解率(ORR)为35.2%。在ATLANTIS试验中,对化疗间隔≥30天且无脑转移的匹配患者人群进行与拓扑替康的间接比较,结果显示鲁比替定具有更高的ORR(41.0% vs 25.5%,p=0.0382)、更长的中位总生存期(mOS)(10.2 vs 7.6个月)和更低的毒性发生率。在ATLANTIS试验中,接受过铂类化疗后复发的SCLC患者,无论接受鲁比替定/多柔比星治疗,还是接受医生选择的静脉注射拓扑替康或CAV方案治疗,其mOS均相似(8.6 vs 7.6个月,p=0.70)。然而,鲁比替定/多柔比星组的毒性较低。由于未直接比较鲁比替定单药与鲁比替定/多柔比星联合用药,因此添加多柔比星的相对获益尚不明确。在一项II期临床试验中,研究人员评估了鲁比替定/伊立替康联合用药在铂类化疗期间或之后出现疾病进展的广泛期小细胞肺癌(ES-SCLC)患者中的疗效。在74例化疗间隔期>30天的患者中,客观缓解率(ORR)为51.4%,中位无进展生存期(mPFS)为5.6个月,中位总生存期(mOS)为12.7个月,表明该联合用药是此类患者中一种有前景的治疗选择。III期LAGOON试验(NCT05153239)正在比较鲁比替定/伊立替康联合用药与鲁比奈德定或拓扑替康单药治疗的疗效。
在小样本患者队列的研究中,紫杉醇、伊立替康和替莫唑胺作为二线及后续治疗方案的单药疗效有限。一项纳入24例铂耐药广泛期小细胞肺癌(ES-SCLC)患者的II期研究显示,紫杉醇的客观缓解率(ORR)为29%,中位总生存期(mOS)为100天。在一项回顾性研究中,185例ES-SCLC患者中93%接受了紫杉醇作为三线或四线治疗,ORR为17%,mOS为3.3个月。在一项针对一线或两线治疗后复发的小细胞肺癌患者的替莫唑胺II期试验中,48例铂敏感患者的ORR为23%,16例铂耐药患者的ORR为22%。在一项II期研究中,30例既往接受过≥1线铂类化疗的患者接受了伊立替康治疗。客观缓解率(ORR)为41.3%,中位无进展生存期(mPFS)为4.1个月,中位总生存期(mOS)为10.4个月。
PD-1和PD-L1免疫检查点抑制剂 (ICI) 已在小细胞肺癌 (SCLC) 的二线和三线治疗中进行过研究,但结果大多为阴性(表3)。CheckMate-331是一项III期临床试验,结果显示,在铂敏感和铂耐药复发性SCLC患者中,纳武利尤单抗的中位总生存期 (mOS) 与拓扑替康或安柔比星化疗相似(7.5个月 vs 8.4个月,p=0.11)。CheckMate-032是一项I/II期临床试验,研究了既往接受过铂类化疗后使用纳武利尤单抗作为三线治疗的疗效,结果显示客观缓解率 (ORR) 为11.9%,12个月总生存期为28.3%。同样,一项I期临床试验研究了帕博利珠单抗在接受过≥2线治疗后用于SCLC的疗效,结果显示ORR为19.3%。然而,这两项研究均未达到mOS终点,因此不推荐用于二线或三线治疗。在II期IFCT-1603试验中,阿特珠单抗作为二线治疗在既往接受过铂类/依托泊苷化疗的患者中疗效不佳,客观缓解率(ORR)为2.3%,尽管中位总生存期(mOS)为9.5个月,而拓扑替康或再次化疗组为8.7个月(p=0.60)。一线化疗联合免疫治疗后再次使用PD-(L)1抑制剂的获益尚不明确,因为PD-(L)1抑制剂的二线治疗试验是在PD-(L)1抑制剂成为一线标准治疗方案之前开展的。
表4总结了目前FDA批准的SCLC系统疗法以及临床试验中报告的相关生存结果。
表4. FDA批准的用于治疗SCLC的全身疗法。
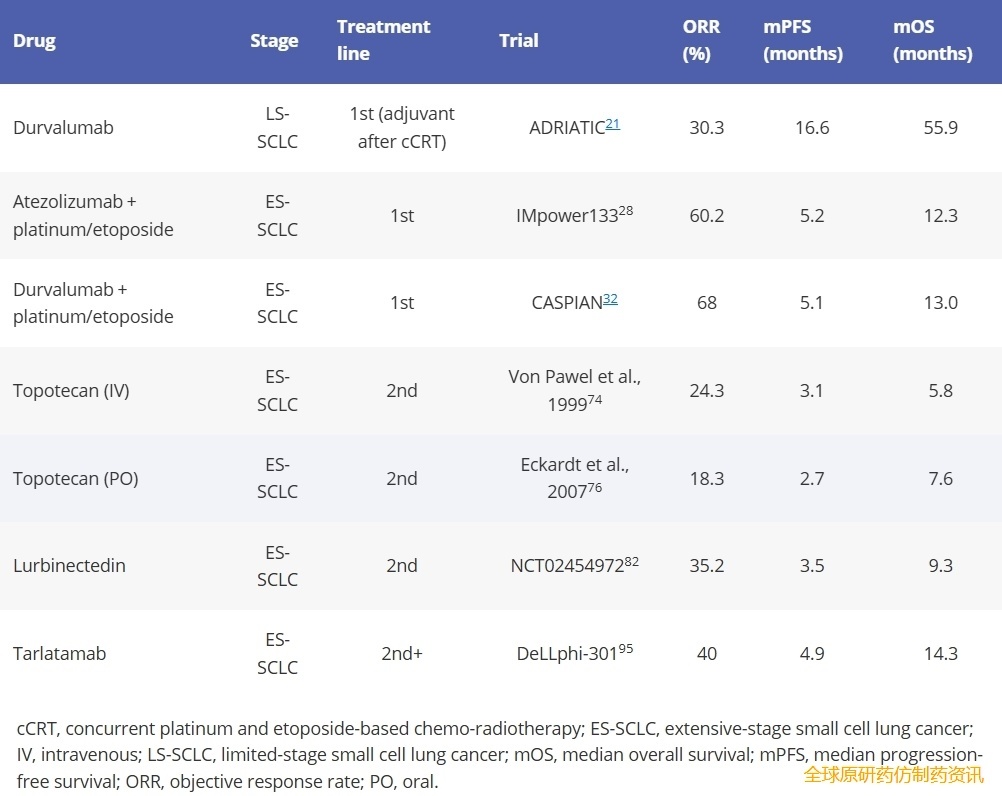
小细胞肺癌的新型靶向疗法
尽管小细胞肺癌(SCLC)最初对铂类化疗敏感,但很快就会产生耐药性,导致疗效短暂,长期预后不良。这促使人们研发旨在克服耐药性并提高疗效持久性的新型疗法。目前,许多药物正在复发或难治性SCLC的研究中,但越来越多的研究致力于将它们纳入一线治疗方案。表5总结了SCLC新型全身治疗和联合治疗的关键临床试验。
表5. 小细胞肺癌新型系统疗法和联合疗法的关键临床试验。
双特异性T细胞衔接器
双特异性抗体(BiTE)是能够同时结合肿瘤细胞表面抗原和T细胞表面CD3的抗体,从而激活T细胞靶向癌细胞并诱导T细胞介导的细胞溶解。Tarlatamab/塔拉妥单抗是一种BiTE,其作用机制是通过靶向小细胞肺癌(SCLC)细胞表面的DLL3和T细胞表面的CD3。在II期DeLLphi-301试验中,220例铂敏感和铂耐药的SCLC患者接受了tarlatamab治疗,这些患者在接受过一线铂类化疗和至少一线其他治疗后复发。接受10 mg剂量治疗的患者客观缓解率(ORR)为40%,接受100 mg剂量治疗的患者为32%,59%的患者缓解持续时间≥6个月。10 mg组的中位无进展生存期(mPFS)为4.9个月,100 mg组为3.9个月;10 mg组的中位总生存期(mOS)为14.3个月,100 mg组尚未达到。细胞因子释放综合征是最常见的毒性反应,10 mg组发生率为51%,100 mg组为61%,主要发生于第一个治疗周期。然而,仅有3%的患者因药物毒性而停止治疗。鉴于其良好的客观缓解率 (ORR) 和良好的毒性特征,tarlatamab于2024年5月获得FDA批准,用于治疗铂类化疗后疾病进展的广泛期小细胞肺癌 (ES-SCLC)。目前,tarlatamab正在III期DeLLphi-304试验中进行进一步评估,作为小细胞肺癌的二线治疗方案,并与标准治疗方案(lurbinectedin、拓扑替康或安柔比星;NCT05740566)进行比较。在DeLLphi-305试验中,该药物也在一线维持治疗环境中进行研究,与durvalumab联合使用,与durvalumab单独使用相比,在卡铂/依托泊苷和durvalumab诱导治疗后使用durvalumab进行比较 (NCT06211036)。
除了tarlatamab之外,其他靶向DLL3的BiTE和T细胞疗法也正在研发中。BiTE BI 764532也是一种DLL3/CD3 T细胞衔接器,目前正在DAREON-5 II期临床试验中研究其作为神经内分泌肿瘤二线及后续治疗方案的疗效,在36例小细胞肺癌(SCLC)患者队列中观察到了令人鼓舞的疗效。进一步的I期临床试验正在探索BI 764532联合铂类/依托泊苷化疗(联合或不联合抗PD-L1疗法)作为一线治疗方案(NCT06132113,NCT06077500),以及联合单药化疗用于复发/难治性SCLC(NCT05990738)。HPN328是一种新型DLL3/CD3 T细胞衔接器,其具有额外的白蛋白结合域,旨在延长其半衰期。在一项针对复发或难治性广泛期小细胞肺癌(ES-SCLC)患者的I/II期临床试验中,HPN328在最初纳入的25例SCLC患者中显示出50%的客观缓解率(ORR)。
迄今为止,BiTE疗法报告的高缓解率支持将其更早地纳入治疗方案——不仅适用于铂类化疗后复发/难治性小细胞肺癌,而且可能适用于一线治疗。需要更多临床数据来全面评估缓解的持久性、对总生存期的影响以及安全性,尤其是在与化疗和/或免疫检查点抑制剂联合使用时。
抗体-药物偶联物
抗体药物偶联物(ADC)目前正在多项临床试验中进行研究,其作用机制是通过抗体递送强效细胞毒性药物,靶向小细胞肺癌(SCLC)中过表达的细胞表面蛋白。罗伐妥珠单抗(Rova-T)是最早用于SCLC研究的ADC之一,它靶向DLL3,并与DNA损伤剂吡咯并苯二氮卓类药物偶联。II期TRINITY研究评估了Rova-T作为三线或后续治疗方案在339例经证实肿瘤中DLL3表达的SCLC患者中的疗效。Rova-T的客观缓解率(ORR)为12.4%,中位总生存期(mOS)为5.6个月。54%的患者出现3-4级毒性反应,10%的患者出现5级毒性反应,其中3%与药物相关。在III期TAHOE研究中,Rova-T与静脉注射拓扑替康作为二线治疗方案在DLL3高表达的广泛期小细胞肺癌(ES-SCLC)患者中进行了比较。接受Rova-T治疗的100例患者的中位总生存期 (mOS) 较拓扑替康治疗的患者更差(6.3个月 vs 8.6个月)。Rova-T的客观缓解率 (ORR) 有限,与标准治疗相比缺乏总生存期获益,且毒性较高,因此未被批准用于小细胞肺癌 (SCLC) 的治疗。
目前正在进行针对Trop-2和其他标志物的新型抗体药物偶联物(ADC)的临床试验。Sacituzumab govitecan是一种ADC,它能与Trop-2结合,并将拓扑异构酶I抑制剂SN-38递送至肿瘤细胞。Trop-2是一种跨膜蛋白,在包括小细胞肺癌(SCLC)在内的多种癌症中过度表达。在II期TROPiCS-03篮式试验中,sacituzumab govitecan作为二线治疗方案,用于治疗既往接受过一线铂类化疗和PD-(L)-1靶向治疗后进展的广泛期小细胞肺癌(ES-SCLC)患者。共有43例患者接受了sacituzumab govitecan治疗,结果显示客观缓解率(ORR)为41.9%,中位无进展生存期(mPFS)为4.4个月,中位总生存期(mOS)为13.6个月。这表明sacituzumab govitecan在二线治疗中具有良好的疗效,需要在III期试验中进行进一步研究。
Ifinatmab deruxtecan (I-DXd) 是一种抗体偶联药物 (ADC),靶向B7-H3,一种在包括小细胞肺癌 (SCLC) 在内的多种肿瘤类型中过度表达的跨膜蛋白,并与拓扑异构酶I抑制剂deruxtecan连接。I-DXd正在研究用于治疗复发/难治性和初治的广泛期小细胞肺癌 (ES-SCLC)。在II期IDeate-Lung01试验 (NCT05280470) 中,纳入了88例既往接受过1-3线治疗(包括铂类化疗)的ES-SCLC患者,I-DXd 12 mg/kg剂量组的客观缓解率 (ORR) 为52.4%,中位无进展生存期 (mPFS) 为5.5个月,中位总生存期 (mOS) 为11.8个月。一项名为IDeate-Lung02(NCT06203210)的III期研究正在比较I-DXd与标准二线化疗(拓扑替康、鲁比替定或安柔比星)的疗效。Ib/II期IDeate-Lung03试验(NCT06362252)正在评估I-DXd联合阿特珠单抗作为一线治疗方案的一部分,用于诱导和维持治疗,可与诱导卡铂/依托泊苷/阿特珠单抗方案同时或在其后使用。
ABBV-796是一种新型抗体偶联药物 (ADC),靶向癫痫相关同源物6 (SEZ6),SEZ6是一种在小细胞肺癌 (SCLC) 中过表达的跨膜蛋白。它与拓扑异构酶I抑制剂偶联,目前正在一项I期临床试验 (NCT05599984) 中进行评估,评估其作为单药疗法以及与布地利单抗(抗PD-1抗体)、卡铂或顺铂联合用药的疗效。来自SCLC患者队列 (n=15) 的初步数据显示,客观缓解率 (ORR) 为40%,表明其在复发/难治性SCLC患者中具有良好的早期临床活性。
总体而言,sacituzumab govitecan和其他抗体偶联药物为小细胞肺癌提供了一种有前景的治疗选择,并取得了令人鼓舞的客观缓解率。它们的更广泛应用将取决于其毒性是否可控以及正在进行的临床试验的进一步验证。
血管生成抑制剂
血管生成抑制剂已被研究作为小细胞肺癌(SCLC)联合治疗方案的一部分。贝伐珠单抗是一种抗VEGF-A单克隆抗体,在多项II期临床研究中与化疗联合用于广泛期小细胞肺癌(ES-SCLC)的疗效评估中,未显示无进展生存期(PFS)或总生存期(OS)的改善。一项在意大利开展的III期随机对照试验(RCT)评估了顺铂/依托泊苷联合或不联合贝伐珠单抗一线治疗ES-SCLC的疗效,结果显示OS未见显著改善。其他大分子抗血管生成药物,如阿柏西普(ziv-aflibercept)和恩度(endostar),以及具有抗VEGF受体(VEGFR)活性的小分子酪氨酸激酶抑制剂(TKI),如舒尼替尼、凡德他尼、索拉非尼、西地尼布和尼达尼布,也已被研究。这些药物与一线化疗联合使用或作为二线及后续治疗的单药,均未能显示OS的显著改善。在中国开展的ALTER1202 II期临床试验中,安罗替尼(一种具有抗VEGFR活性的多激酶抑制剂)在接受过≥2线化疗后复发的铂耐药或铂敏感小细胞肺癌(SCLC)患者中,与安慰剂相比,显著改善了中位总生存期(mOS)(7.3个月 vs 4.9个月,p=0.0029)。尽管疾病控制率高达66.7%,但客观缓解率(ORR)仅为4.9%。目前,安罗替尼已在中国获批用于SCLC的三线及以上治疗。
血管生成抑制剂也已与化疗免疫疗法联合应用进行研究。在中国开展的III期ETER701试验研究了安罗替尼联合苯美司巴(抗PD-L1抗体)联合卡铂/依托泊苷一线治疗广泛期小细胞肺癌(ES-SCLC)的疗效,并与安罗替尼联合安慰剂联合卡铂/依托泊苷以及双安慰剂联合卡铂/依托泊苷进行比较。苯美司巴和安罗替尼联合卡铂/依托泊苷可显著延长中位总生存期(mOS)(19.3个月 vs 11.9个月, p=0.0002)。然而,仅在卡铂/依托泊苷方案中加入安罗替尼并未显著延长mOS(13.3个月 vs 11.9个月,p=0.1723)。这表明,联合免疫检查点抑制剂(ICI)可能增强血管生成抑制剂的疗效。一项关键的局限性在于缺乏单独使用PD-L1抑制剂联合卡铂/依托泊苷的治疗组,而这才是目前标准治疗方案的代表。尽管如此,该试验提示,在化疗联合免疫治疗方案中加入血管生成抑制剂可能带来总生存期(OS)获益。目前,苯莫司托巴和安罗替尼联合铂类/依托泊苷已在中国获批用于广泛期小细胞肺癌(ES-SCLC)的一线治疗。一项Ib/II期临床试验进一步证实了血管生成抑制剂联合化疗联合免疫治疗一线治疗的有效性。该试验评估了舒鲁法替尼(一种具有抗VEGFR活性的多激酶抑制剂)和PD-1抑制剂托瑞普利单抗联合顺铂/依托泊苷用于ES-SCLC一线治疗的疗效。该试验纳入了35例患者,报告的中位无进展生存期(mPFS)为6.9个月,中位总生存期(mOS)为21.1个月。血管生成抑制剂与免疫检查点抑制剂(ICI)联合治疗也在二线治疗中进行研究。在一项II期临床试验中,接受过至少一线铂类化疗的小细胞肺癌(SCLC)患者接受了PD-1抑制剂信迪利单抗联合安罗替尼治疗。在37例患者中,客观缓解率(ORR)为56.8%,中位无进展生存期(mPFS)为6.1个月,中位总生存期(mOS)为12.7个月。在PASSION II期临床试验中,接受过一线化疗的广泛期小细胞肺癌(ES-SCLC)患者接受了PD-1抑制剂卡瑞利珠单抗联合VEGFR2抑制剂阿帕替尼治疗,结果显示mPFS为3.6个月,mOS为8.4个月。在铂敏感患者和铂耐药患者中,ORR(37.5% vs 32.3%)、mPFS(3.6 vs 2.7个月)和mOS(9.6 vs 8.0个月)均相似。这些研究表明,将血管生成抑制剂与免疫检查点抑制剂联合使用,可能对一线治疗及后续治疗均有益处。
PARP抑制剂
聚(ADP-核糖)聚合酶抑制剂(PARPi)已被研究作为小细胞肺癌(SCLC)一线和维持治疗联合疗法的一部分。在II期ECOG-ACRIN 2511试验中,与安慰剂联合顺铂/依托泊苷相比,维利帕尼联合顺铂/依托泊苷一线治疗广泛期小细胞肺癌(ES-SCLC)显著改善了中位无进展生存期(mPFS)(6.1个月 vs 5.5个月,p=0.01),但未显著改善中位总生存期(mOS)(10.3个月 vs 8.9个月,p=0.17)或客观缓解率(ORR)(71.9% vs 65.6%,p=0.57)。在另一项II期试验中,维利帕尼联合铂类/依托泊苷一线治疗后序贯维利帕尼维持治疗,与安慰剂联合铂类/依托泊苷相比,未改善mPFS或mOS。进一步的研究探讨了PARP抑制剂作为一线维持治疗的疗效。II期SWOG S1929试验比较了SLFN11阳性广泛期小细胞肺癌(ES-SCLC)患者一线治疗后,接受他拉唑帕尼联合阿特珠单抗维持治疗与单用阿特珠单抗维持治疗的疗效。该联合治疗方案使中位无进展生存期(mPFS)有轻微但具有统计学意义的改善(2.9个月 vs 2.4个月,HR=0.66,p=0.019),但初步结果显示中位总生存期(mOS)无显著差异。该试验为基于小细胞肺癌亚型的生物标志物导向的试验设计奠定了基础。在STOMP II期试验中,对一线治疗有反应的局限期小细胞肺癌(LS-SCLC)或广泛期小细胞肺癌(ES-SCLC)患者被随机分配接受奥拉帕尼或安慰剂维持治疗,结果显示两组在mPFS或mOS方面均无显著差异。同样,在中国开展的ZL-2306-005 II期临床试验中,对于一线铂类化疗有效的广泛期小细胞肺癌(ES-SCLC)患者,尼拉帕尼维持治疗与中位无进展生存期(mPFS)略有延长相关(1.54个月 vs 1.36个月,p=0.024),但中位总生存期(mOS)无显著差异(9.92个月 vs 11.43个月,p=0.905)。
PARP抑制剂也在二线及后续治疗中进行研究。在一项II期临床试验中,研究人员比较了维利帕尼联合替莫唑胺与单用替莫唑胺治疗复发性铂敏感或铂耐药小细胞肺癌(SCLC)患者的疗效。虽然维利帕尼联合替莫唑胺组的客观缓解率(ORR)更高(39% vs 14%,p=0.016),但4个月无进展生存期(PFS)和中位总生存期(mOS)均未见显著改善。同样,一项针对既往接受过治疗的SCLC患者的I/II期临床试验也研究了奥拉帕尼联合替莫唑胺的疗效,并取得了令人鼓舞的结果:ORR为41.7%,mPFS为4.2个月,mOS为8.5个月。在I/II期MEDIOLA试验中,奥拉帕尼联合度伐利尤单抗治疗铂类化疗后复发的小细胞肺癌患者,客观缓解率 (ORR) 为10.5%,中位无进展生存期 (mPFS) 为2.4个月,提示PARP抑制剂联合免疫检查点抑制剂 (ICI) 的疗效有限,尽管中位总生存期 (mOS) 为7.6个月。
总体而言,虽然PARP抑制剂(如维利帕尼和奥拉帕尼)与化疗联合使用时,在提高客观缓解率(ORR)和无进展生存期(PFS)方面显示出一定的潜力,但迄今为止,它们尚未在总生存期(OS)方面显示出显著改善。SLFN11等生物标志物可能在预测哪些患者可能从PARP抑制剂治疗中获益方面发挥重要作用,但仍需开展更多研究来确定PARP抑制剂在小细胞肺癌(SCLC)治疗中的作用。
ATR抑制剂
在一项针对既往接受过≥1种化疗方案后复发的SCLC患者的II期临床试验中,研究人员比较了ATR抑制剂berzosertib联合拓扑替康与单用拓扑替康的疗效。在57例患者中,客观缓解率(ORR)(26% vs 6%,p=0.15)和中位无进展生存期(mPFS)(3.9个月 vs 3.0个月,p=0.44)均无显著差异。然而,berzosertib联合拓扑替康组的中位总生存期(mOS)显著长于单用拓扑替康组(8.9个月 vs 5.4个月,p=0.03),提示该联合治疗方案具有良好的应用前景,且在铂敏感和铂耐药亚组中疗效相似。
新兴治疗靶点
近年来,高分辨率组学技术(包括单细胞和空间转录组学)的进步,以及生物信息学和人工智能的发展,显著提升了我们对小细胞肺癌(SCLC)分子异质性、亚型以及驱动表型可塑性和治疗耐药性的机制的理解。这些工具与临床前体外和体内模型相结合,正被用于识别系统性治疗的新靶点。
靶向MYC家族基因是小细胞肺癌(SCLC)治疗领域的新兴策略。MYC家族基因扩增通过NOTCH信号通路促进细胞增殖和从神经内分泌表型向非神经内分泌表型的转分化,而NOTCH信号通路是化疗耐药的关键机制。Aurora激酶可稳定MYC蛋白,其抑制可导致MYC降解和肿瘤细胞凋亡(临床前模型)。同样,USP7抑制剂已被证实可逆转MYCN过表达小鼠模型中的铂类/依托泊苷耐药性。这些发现凸显了Aurora激酶和USP7作为MYC家族驱动型SCLC潜在治疗靶点的重要性。
表观遗传失调是小细胞肺癌(SCLC)的标志性特征,也是一条极具潜力的治疗途径。EZH2通过H3K27me3沉默肿瘤抑制基因并下调MHC I类分子,从而促进肿瘤细胞的免疫逃逸。它还抑制SLFN11的表达,而SLFN11是决定肿瘤细胞对DNA损伤药物敏感性的关键因素。在SCLC小鼠模型中,抑制EZH2可恢复SLFN11的表达和抗原呈递,使肿瘤细胞重新对拓扑异构酶抑制剂敏感,并预防获得性耐药的产生。LSD1是另一个新兴的表观遗传靶点。它通过抑制NOTCH信号通路和炎症基因的表达来维持神经内分泌表型。抑制LSD1可破坏这种抑制作用,使肿瘤细胞向炎症表型转变,并在临床前模型中增强对PD-1抑制剂的疗效。
CDK7抑制是提高免疫检查点抑制剂(ICI)疗效的另一种潜在策略。CDK7调控细胞周期进程,选择性抑制CDK7可诱导复制应激和基因组不稳定,从而触发免疫信号传导和T细胞介导的肿瘤监视。在小细胞肺癌(SCLC)临床前模型中,CDK7抑制与抗PD-1疗法具有协同作用,可改善肿瘤控制和提高生存率。
新型免疫治疗方法也在研究中。靶向DLL3的CAR-T细胞(例如AMG 119)已进入早期临床试验,并显示出令人鼓舞的早期活性和耐受性迹象。
染色体外DNA(ecDNA)存在于约20%的小细胞肺癌(SCLC)肿瘤中,与肿瘤侵袭性增强、非染色体遗传导致的异质性增加以及预后不良相关。在SCLC小鼠模型中,携带MYC家族基因扩增的ecDNA与获得性耐药和对DNA损伤化疗的交叉耐药相关。ecDNA阳性肿瘤通常表现出复制应激和转录-复制冲突,在临床前研究中对CHK1抑制剂表现出选择性敏感性。因此,ecDNA既可作为SCLC治疗耐药性的生物标志物,也可作为治疗靶点。
这些新兴的治疗策略标志着治疗策略正朝着基于机制、生物标志物指导的方法转变,以克服化疗和免疫疗法的耐药性,凸显了生物标志物在指导治疗选择和实现小细胞肺癌个性化治疗方面的必要性。
小细胞肺癌治疗选择中预测性和预后性生物标志物的现状
尽管小细胞肺癌(SCLC)具有异质性,但目前SCLC的治疗缺乏基于分子亚型或生物标志物的分层方法。全基因组测序研究表明,SCLC肿瘤中存在高比例的异质性体细胞基因突变。然而,迄今为止,突变谱分析未能识别出不同的亚型或可靶向的治疗靶点,且在预测治疗反应方面的应用有限。因此,迫切需要能够预测现有及新兴疗法疗效、实现个体化治疗并改善生存预后的生物标志物。图1展示了近期临床研究中探索的候选治疗反应生物标志物。
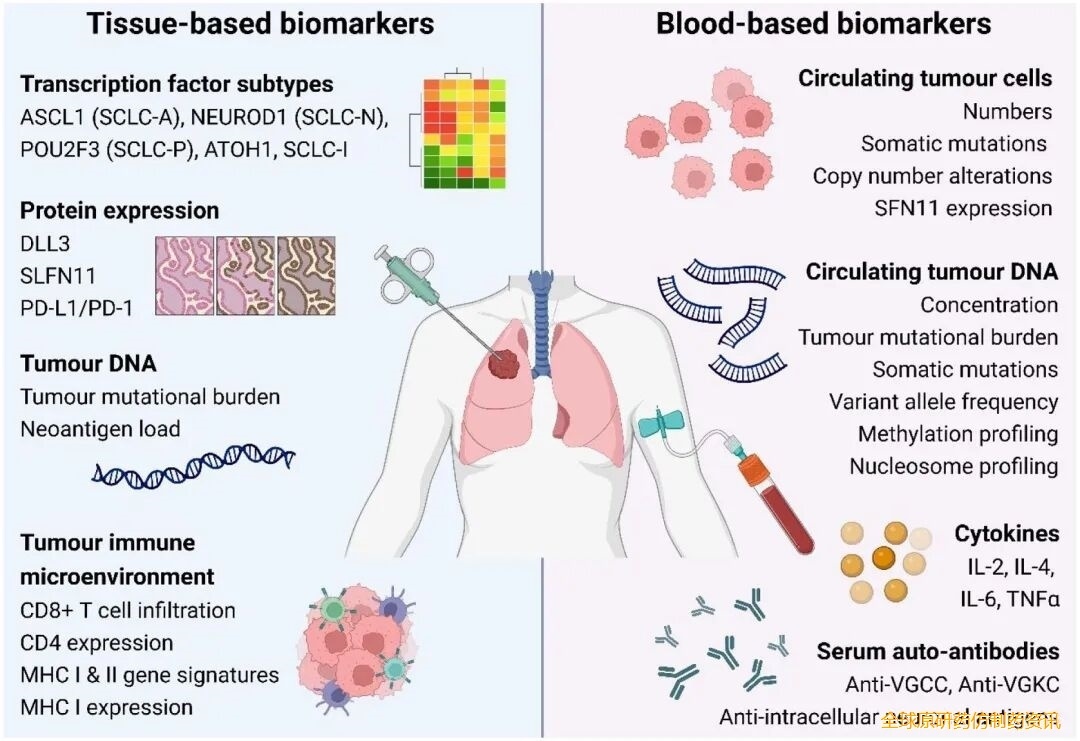
图1. 临床研究中调查的用于小细胞肺癌治疗选择的基于组织和基于血液的候选生物标志物。
转录亚型
临床前研究表明,小细胞肺癌(SCLC)的转录亚型可能对全身治疗具有不同的敏感性,凸显了它们作为指导治疗选择的生物标志物的潜力。在IMpower133试验中,SCLC-I亚型患者在化疗联合阿特珠单抗治疗后,中位总生存期(mOS)改善最为显著(18个月 vs 10个月),提示其对PD-L1抑制剂的生存获益具有预测价值。同样,在CASPIAN试验中,接受度伐利尤单抗±曲美木单抗/卡铂/依托泊苷治疗的SCLC-I亚型患者的mOS最长,为24.0个月,而SCLC-N、SCLC-A和SCLC-P亚型患者的mOS分别为12.1个月、11.5个月和7.0个月。在IMpower133研究中,SCLC-A和SCLC-N亚型中发现肿瘤DLL3高表达,提示其可能对靶向DLL3的药物敏感。SCLC-A亚型可根据SLFN11表达水平的高低进一步分层,SLFN11是DNA损伤药物疗效的潜在生物标志物。体外实验表明,SCLC-A对BCL2抑制剂敏感,SCLC-N对Aurora激酶抑制剂敏感,SCLC-I对BTK抑制剂敏感,而SCLC-P对顺铂、PARP抑制剂和抗代谢药物敏感。需要开展包含转录亚型分析的前瞻性临床研究,以确定其在预测全身治疗反应方面的临床应用价值。
免疫治疗反应的生物标志物
肿瘤组织中PD-L1的表达被广泛用作非小细胞肺癌(NSCLC)和其他癌症中免疫检查点抑制剂(ICIs)疗效的预测性生物标志物。在IMpower和CASPIAN试验中,肿瘤中PD-L1的表达主要存在于免疫细胞而非肿瘤细胞中,且表达水平通常较低且变异性较大。在这些试验中,PD-L1表达并不能预测在化疗方案中加入PD-L1抑制剂后的客观缓解率(ORR)、无进展生存期(PFS)或总生存期(OS)。同样,基于血液的肿瘤突变负荷(TMB)也不能预测在化疗方案中加入抗PD-L1疗法后的OS获益。然而,在CASPIAN试验中,PD-L1表达能够预测在卡铂/依托泊苷方案中加入PD-L1和CTLA-4抑制剂后OS的改善。在CheckMate-032试验中,高TMB患者的客观缓解率(ORR)高于低TMB患者:伊匹木单抗/纳武单抗组为46.2% vs 22.2%,纳武单抗组为21.3% vs 4.8%。伊匹木单抗/纳武单抗组和纳武单抗单药组高TMB患者的1年总生存期(OS)也均长于低TMB患者(分别为62.4% vs 19.6%和35.2% vs 22.1%)。这表明TMB可以预测免疫检查点抑制剂(ICI)的生存获益。
肿瘤免疫细胞特征也可能有助于预测免疫检查点抑制剂(ICI)的疗效。IMpower133研究中治疗前小细胞肺癌(SCLC)样本显示,基于免疫基因特征,SCLC-I亚型可分为神经内分泌亚型和非神经内分泌亚型。SCLC-I神经内分泌亚型的特征是肿瘤相关巨噬细胞信号低但效应T细胞信号高,与单用卡铂/依托泊苷相比,阿特珠单抗联合卡铂/依托泊苷可显著延长总生存期(OS)(HR=0.26,95% CI,0.12–0.57)。在非神经内分泌SCLC-I亚型中,肿瘤相关巨噬细胞和效应T细胞信号均较高,各组间OS差异不大(HR=0.85,95% CI,0.53–1.37)。这表明特定的SCLC-I亚型可能预示着PD-L1抑制剂免疫疗法能改善生存率。
其他免疫相关生物标志物也已被探索。在一项回顾性研究中,研究人员根据PD-1表达和CD8+肿瘤浸润淋巴细胞(TIL)密度,将135例既往接受过治疗的广泛期小细胞肺癌(ES-SCLC)肿瘤分为炎症型和非炎症型。研究人员采用全外显子组测序评估了137例肿瘤新抗原负荷。与单纯化疗相比,接受化疗联合免疫治疗的炎症型肿瘤患者的中位无进展生存期(mPFS)更长(10.8个月 vs 5.1个月, p=0.002)。高移码新抗原负荷患者的12个月无进展生存期更长(16.1% vs 0%)。这表明,肿瘤中PD-1表达、CD8+T细胞浸润和新抗原负荷可能预测免疫检查点抑制剂(ICI)的疗效。对CASPIAN试验中182例治疗前肿瘤样本的分析表明,CD8A表达/CD8细胞密度、CD4表达、抗原呈递/加工机制、MHC I和II基因特征以及较高的MHC I表达水平与低CD8A表达水平相比,可预测在化疗-免疫疗法中加入tremelimumab/曲美木单抗后患者的总生存期获益。
血清自身免疫抗体和细胞因子已显示出预测伊匹木单抗疗效的潜力。在一项II期临床试验中,研究人员比较了47例接受伊匹木单抗联合卡铂/依托泊苷治疗的患者和38例仅接受卡铂/依托泊苷治疗的患者的血清抗电压门控钙通道抗体、抗电压门控钾通道抗体以及抗细胞内神经元抗原抗体水平。结果显示,基线自身免疫抗体阳性的患者在接受伊匹木单抗治疗后,中位无进展生存期(mPFS)显著延长(8.8个月 vs 7.3个月,p=0.036),但中位总生存期(mOS)无显著差异。此外,伊匹木单抗联合化疗也普遍升高了血清细胞因子水平。基线IL-2水平升高预示着对伊匹木单抗的敏感性,而IL-6和TNF-α水平升高则预示着耐药性。接受化疗联合免疫治疗的患者中IL-4水平升高与总生存期(OS)的改善相关。这些研究结果受限于样本量小、独立且不匹配的队列,以及对CTLA-4抑制剂的关注,而CTLA-4抑制剂目前并未用于SCLC的标准治疗。
靶向治疗反应的生物标志物
由于靶向DLL3疗法的开发,DLL3作为一种预测性生物标志物备受关注。尽管DLL3在小细胞肺癌(SCLC)中广泛表达,但其表达具有异质性。在II期Rova-T研究中,DLL3高表达(≥75%肿瘤细胞)和治疗前DLL3阳性肿瘤患者的客观缓解率(ORR)相似(分别为14.3%和13.2%)。在DeLLphi-301研究中,DLL3阳性和阴性患者均对tarlatamab治疗有反应。这提示DLL3表达水平可能无法预测对DLL3靶向疗法的反应。需要开展更大规模队列研究,并改进DLL3分层,以证实这些发现。
SLFN11已成为多种癌症和临床前小细胞肺癌 (SCLC) 模型中DNA损伤疗法的潜在预测性生物标志物。在一项II期临床试验中,接受维利帕尼/替莫唑胺治疗的SLFN11阳性且既往接受过治疗的SCLC肿瘤,与SLFN11阴性肿瘤相比,显示出更长的中位无进展生存期 (mPFS)(5.7个月 vs 3.6个月,p=0.009)和中位总生存期 (mOS)(12.2个月 vs 7.5个月,p=0.014)。无论SLFN11表达如何,单独使用替莫唑胺治疗均未观察到mPFS或mOS的差异。这提示SLFN11可能预测维利帕尼的疗效。利用小细胞肺癌(SCLC)细胞系和异种移植模型进行的临床前研究表明,SLFN11低表达与对鲁比替定(lurbinectedin)的耐药性相关,而SLFN11缺失则与对ATR抑制剂的敏感性增加相关。这提示SLFN11可能具有作为预测对鲁比替定和ATR抑制剂疗效的生物标志物的潜力。在一项II期临床试验中,携带O-6-甲基鸟嘌呤-DNA甲基转移酶(MGMT)DNA修复基因甲基化的复发性SCLC患者中,38%对替莫唑胺治疗有反应,而MGMT未甲基化的患者中仅有7%有反应,这提示MGMT甲基化可能作为替莫唑胺疗效的生物标志物,这与胶质母细胞瘤的研究结果一致。
液体活检
由于小细胞肺癌(SCLC)肿瘤组织来源有限,人们对基于血液的液体活检作为一种微创的肿瘤分子特征分析方法越来越感兴趣。循环肿瘤细胞(CTC)和循环肿瘤DNA(ctDNA)分别在70%–95%和>90%的小细胞肺癌患者血液中被检测到,这表明它们作为预测和监测治疗反应的生物标志物具有巨大的潜力。
循环肿瘤细胞(CTC)数量升高与接受铂类化疗患者的无进展生存期(PFS)和总生存期(OS)较差相关,尽管大多数研究并未显示CTC计数变化与肿瘤反应之间存在显著相关性。在接受放化疗的局限期小细胞肺癌(LS-SCLC)患者中,较高的CTC水平与较差的PFS和OS相关。CTC的单细胞测序可以识别体细胞突变和/或拷贝数变异(CNA),CNA评分可以预测一线化疗患者的PFS和OS。检测CTC中SLFN11的表达已显示出预测和监测DNA损伤疗法疗效的潜力。CTC上的PD-L1表达也正在被探索作为免疫检查点抑制剂(ICI)疗效的生物标志物。
小细胞肺癌(SCLC)患者的游离DNA(cfDNA)可通过突变、甲基化、片段化和/或结构改变的分析进行研究。高水平的ctDNA与较差的无进展生存期(PFS)和总生存期(OS)相关。ctDNA突变谱分析已鉴定出可靶向的突变和化疗耐药机制,但这些尚未证实其在匹配靶向治疗方面的实用性。血液肿瘤突变负荷(TMB)的降低与更好的预后相关,根治性治疗后可检测到的ctDNA预示着更差的PFS和OS。cfDNA突变的纵向研究表明,变异等位基因频率和血液TMB随化疗而降低,ctDNA水平的变化与化疗反应相关。全基因组拷贝数变异(CNA)的纵向分析表明,其可检测性与化疗反应和复发/进展相关。这些研究大多受限于样本量小,并且突变谱分析在小细胞肺癌的分子分型和治疗分层方面缺乏实用性。
人们对cfDNA的表观基因组分析在亚型分型、监测、预后和预测治疗反应方面的兴趣日益浓厚。cfDNA的甲基化谱分析已被证明可用于识别小细胞肺癌(SCLC)的转录亚型,cfDNA突变谱和核小体谱的联合分析也显示出类似的应用价值。这种方法能够以微创方式识别SCLC的转录亚型,未来可能对治疗分层和亚型转换的纵向监测具有重要价值。cfDNA的甲基化谱和核小体谱的联合分析也显示出检测EGFR突变型非小细胞肺癌(NSCLC)向SCLC转化的潜力,这有助于更早地识别转化并指导治疗方案的调整。因此,cfDNA作为一种微创肿瘤亚型分型和监测工具,在辅助治疗选择方面具有巨大的潜力。
结论
药物研发的进步和对小细胞肺癌(SCLC)亚型认识的不断深入,正逐步重塑治疗格局,使其朝着更有效、更个体化的治疗方向发展。近期进展包括在广泛期小细胞肺癌(ES-SCLC)化疗中加入免疫检查点抑制剂(ICIs),以及在局限期小细胞肺癌(LS-SCLC)根治性放化疗后将其作为辅助治疗。ICIs目前也在评估其与放化疗联合应用或作为LS-SCLC巩固治疗的疗效。然而,由于耐药性的快速发展和高复发率,ICIs的疗效仍然不佳,仅有少数患者能从中获得长期生存获益。
除一线治疗外,化疗方案如鲁比替定、拓扑替康和铂类/依托泊苷再挑战治疗可带来有限的生存获益。靶向DLL3的双特异性抗体(BiTE)tarlatamab已证实可显著改善生存结局,并已获得FDA批准用于复发性小细胞肺癌(SCLC),目前正在早期治疗中进行研究。其他BiTE也正在研发中,并已取得令人鼓舞的早期结果。包括sacituzumab govitecan和I-DXd在内的几种抗体偶联药物(ADC)正在进行临床研究,并在既往接受过治疗的SCLC患者中显示出令人鼓舞的疗效。PARP抑制剂和血管生成抑制剂作为SCLC单药治疗的疗效目前有限,但联合治疗(例如与免疫检查点抑制剂联合使用)可能带来更大的获益。
分子谱分析和计算生物学正在加深我们对小细胞肺癌(SCLC)亚型的理解,揭示治疗耐药机制,并有助于识别新的治疗靶点。最终,可能需要基于机制的联合治疗策略来克服耐药性并实现持久疗效。在治疗早期引入新型疗法以延缓或预防耐药性并降低复发风险,很可能成为未来的研究重点。尽管目前临床实践中尚未应用任何预测性生物标志物或分子亚型,但正在研究的候选标志物包括转录亚型、SLFN11、肿瘤突变负荷(TMB)、免疫特征和液体活检。我们仍然迫切需要更有效的疗法、更完善的分子分型方法和可靠的生物标志物,以优化治疗方案的选择并实现SCLC治疗的个体化。
点击“转发”吧
生成海报
 长按扫码关注公众号
长按扫码关注公众号