胶质母细胞瘤是成人中最具侵袭性的原发性恶性脑肿瘤。目前其标准治疗(SOC)包括手术、放疗及替莫唑胺等,但在此标准治疗方案下,患者的中位总生存期(mOS)仅为 15-17 个月,临床上因此迫切需要探索新的治疗方向。
近年来,免疫疗法凭借免疫细胞可转运至肿瘤部位、并摧毁浸润性肿瘤细胞的潜在能力,成为对抗这类顽疾颇具吸引力的研究方向。其中,树突状细胞(DC)作为免疫系统的核心组成部分,更是调控免疫耐受与免疫应答的关键角色。
《转化医学杂志》报道了自体树突状细胞疫苗(DCVax®-L)治疗新诊断胶质母细胞瘤的大型 III 期临床试验(NCT00045968)首批生存结果。该研究不仅为胶质母细胞瘤患者带来了全新希望,更再次印证了癌症疫苗在难治性肿瘤治疗领域的巨大潜力,为深陷困境的患者点亮了生命之光!
▲截图源自“BMC”
该研究(NCT00045968)共纳入331例新诊断的胶质母细胞瘤患者,构成意向治疗(ITT)人群。患者在接受手术与放化疗后,按2:1的比例随机分组,分别接受替莫唑胺联合DCVax-L治疗(n=232)或替莫唑胺联合安慰剂治疗(n=99)。
结果显示:本次分析时,331例患者中仍有108例(32.6%)存活。意向治疗(ITT)人群(n=331)的中位生存期(mOS)为手术后23.1个月(95%CI:21.2-25.4),2年和3年生存率分别为46.2%、25.4%(详见下图)。
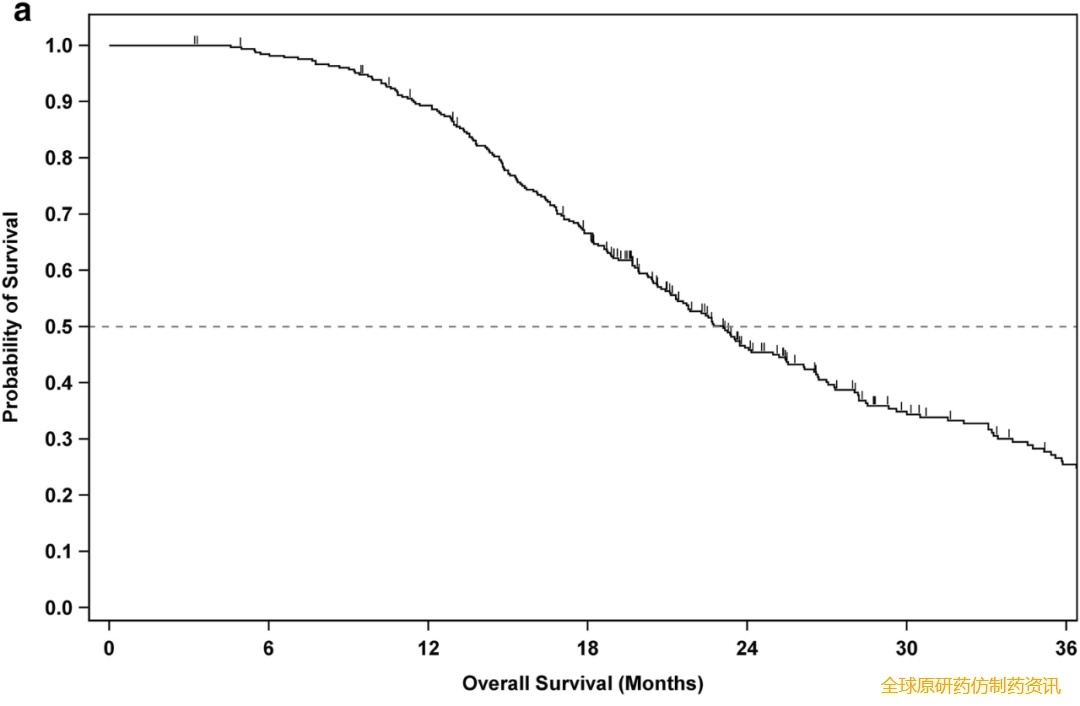
▲图源“BMC”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,在标准治疗(SOC)中添加DCVax-L自体树突状细胞疫苗,对胶质母细胞瘤患者而言不仅可行且安全,还能延长其生存期。
除上文提及的脑瘤DC癌症疫苗外,近期由纪念斯隆凯瑟琳癌症中心研发的KRAS突变靶向疫苗ELI-0022P,同样引发广泛关注。
KRAS突变曾长期被视为“不可成药”靶点——约20%-25%的人类肿瘤存在该促癌驱动突变,在结直肠癌(50%)、胰腺导管腺癌(93%)中高发,还涉及肺癌、肝癌、甲状腺癌等多癌种。尽管近年KRASG12C靶向药问世,但多数患者数月内即耐药;且KRAS突变肿瘤经标准局部治疗后易复发,复发后多依赖姑息治疗,5年生存率仅23.3%,临床仍深陷“难治愈、易进展”的困境。
而ELI-0022P疫苗成功打破了这一魔咒。作为一款针对KRAS突变的治疗型疫苗,其核心适应症为KRAS突变阳性实体瘤(尤其胰腺导管腺癌、结直肠癌),设计极具巧思:将两种KRAS突变抗原肽(G12D、G12V)与TLR9激动剂连接在可结合白蛋白的脂质上,借助白蛋白“转运”进入淋巴结,从而更高效激活针对KRAS突变的适应性免疫。更关键的是,它具备“无需单独设计”的独特优势,可直接激活免疫系统攻击癌细胞,既省去复杂定制流程,又大幅缩短制备时间,为病情急迫的患者带来新希望。
▼癌症疫苗帮助训练T细胞(蓝色)攻击肿瘤细胞
▲图源“UCLA”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
这款疫苗的I期临床试验AMPLIFY-201(NCT04853017)振奋数据已同步发表于全球知名期刊《Nature Medicine》。研究共纳入25例18岁以上的mKRAS G12D/G12R突变患者(含20例胰腺癌、5例结直肠癌),均为经标准局部治疗后,因MRD(ctDNA阳性或CA19-9/CEA升高)存在高复发风险者;入组后患者接受靶向淋巴结的ELI-0022P单药治疗,中位随访时长19.7个月。
结果显示:全队列中位总生存期(mOS)达28.94个月(详见下图a),中位无复发生存期(mRFS)为16.33个月(详见下图b)。其中胰腺癌亚组表现尤为突出,mOS与全队列一致(28.94个月),mRFS达15.31个月,显著优于历史数据——术后ctDNA阳性胰腺癌患者的中位RFS仅5.0-6.37个月、OS仅17.0个月。此外,16/20胰腺癌患者、5/5结直肠癌患者治疗后肿瘤标志物明显降低。
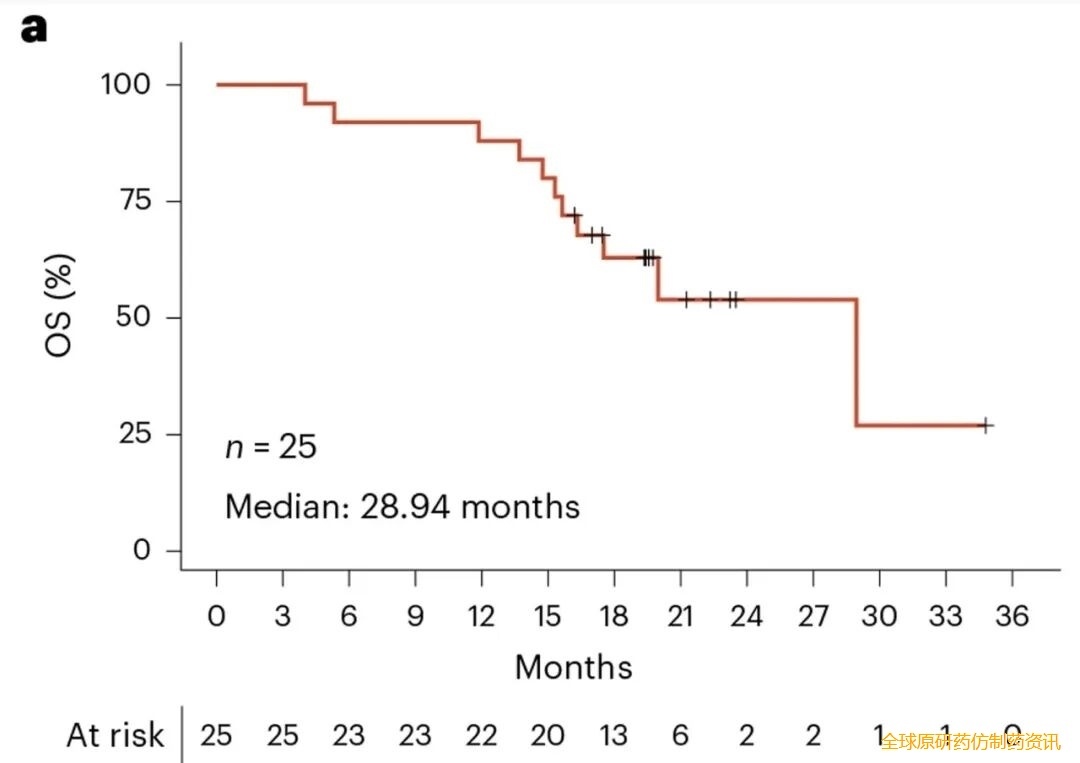
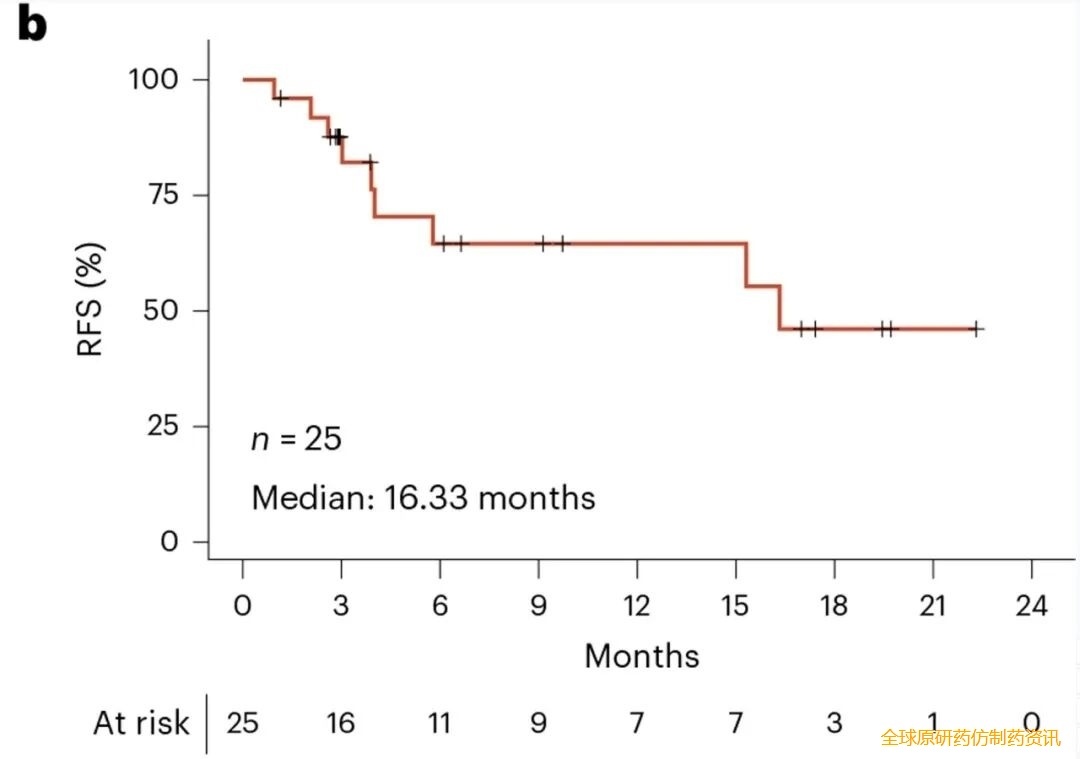
▲图源“Nat Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
目前,癌症疫苗中临床疗效及预防复发效果较突出的是树突状细胞疫苗、mRNA癌症疫苗、古巴肺癌疫、个性化新抗原疫苗等。
1、树突状细胞(DC)疫苗:在日本、德国等,用于临床辅助治疗多种癌症,包括皮肤癌、肝癌、肺癌、肾癌、乳腺癌等,是癌症患者的新希望!
2、mRNA癌症疫苗:正在针对肺鳞癌、肝癌、结直肠癌、黑色素瘤、食道癌、三阴性乳腺癌、头颈部肿瘤等多款恶性实体瘤,开展临床研究。
3、古巴肺癌疫苗(CIMAvax-EGF):中国患者现无需出国,可通过全球肿瘤医生网医学部,向古巴医疗部门申请肺癌疫苗,以延长生存期,提高生活质量!
想寻求国内外癌症疫苗或其他治疗新技术帮助的患者,可先将治疗经历、病理报告、出院小结等资料,提交到全球肿瘤医生网医学部(400-666-7998),进行初步评估或了解详细的入排标准。
同样在2025年,《Nature Medicine》还报道了另一款疗效亮眼的疫苗——BNT122(又名自基因cevumeran、RO7198457)。这是一款个体化新抗原mRNA疫苗,可编码20余种特异性新抗原,其设计核心是基于每位患者肿瘤组织中的肿瘤特异性体细胞突变数据,通过刺激机体产生针对多达20种新抗原的T细胞反应,从而降低肿瘤复发风险、延长患者生存期。
在1期GO39733临床研究(NCT03289962)中,一位肾癌患者(患者38)的治疗效果尤为振奋人心。该患者在入组前已接受过包括纳武单抗在内的4种全身治疗,入组初期病情曾出现进展,但后续成功达到部分缓解(PR)。其胸膜靶病变的最长直径总和(SLD)在基线时为108mm,治疗13个月后缩小至10mm(详见下图),肿瘤显著缩小近10倍。
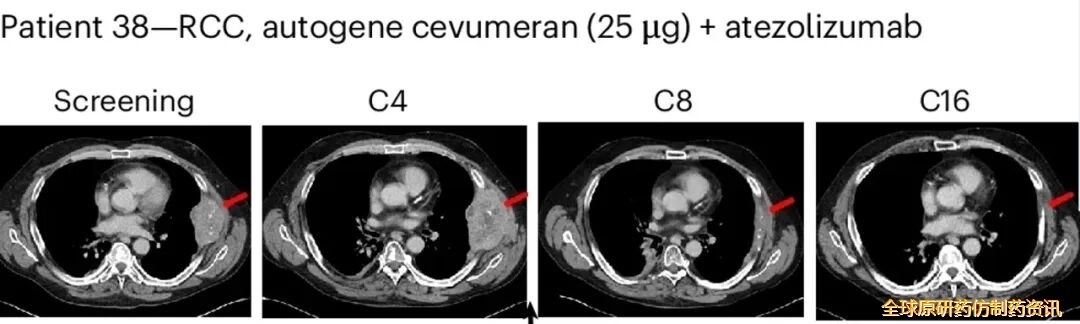
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
癌症疫苗除了“单打独斗”外,还可与放疗、化疗、NK细胞治疗等其他疗法联用,以增强抗癌效果。此处以BI1361849联合局部放疗治疗肺癌为例,该研究直观展现了这一协同效应。
BI1361849(CV9202)是一种活性癌症免疫治疗药物,其核心成分为经鱼精蛋白配制的序列优化mRNA,可编码非小细胞肺癌相关的6种抗原(MUC-1、MAGE-C1、MAGE-C2、NY-ESO-1、5T4、survivin),旨在诱导机体产生靶向这些抗原的免疫反应。
《癌症免疫治疗杂志》曾报道其Ib期临床试验(NCT01915524)结果——该试验纳入26例年龄≥18岁的IV期非小细胞肺癌(NSCLC)患者,专门评估该联合方案的疗效。
结果显示:从首次BI1361849治疗开始,患者中位无进展生存期(PFS)为2.87个月(详见下图a),中位总生存期(OS)为13.95个月(详见下图b);其中46.2%(12/26)的患者达到病情稳定(SD);截至末次随访,1例患者已确认达到部分缓解(PR)且肿瘤缩小可测量,另有6例患者未接受放射治疗的病变缩小超过15%。
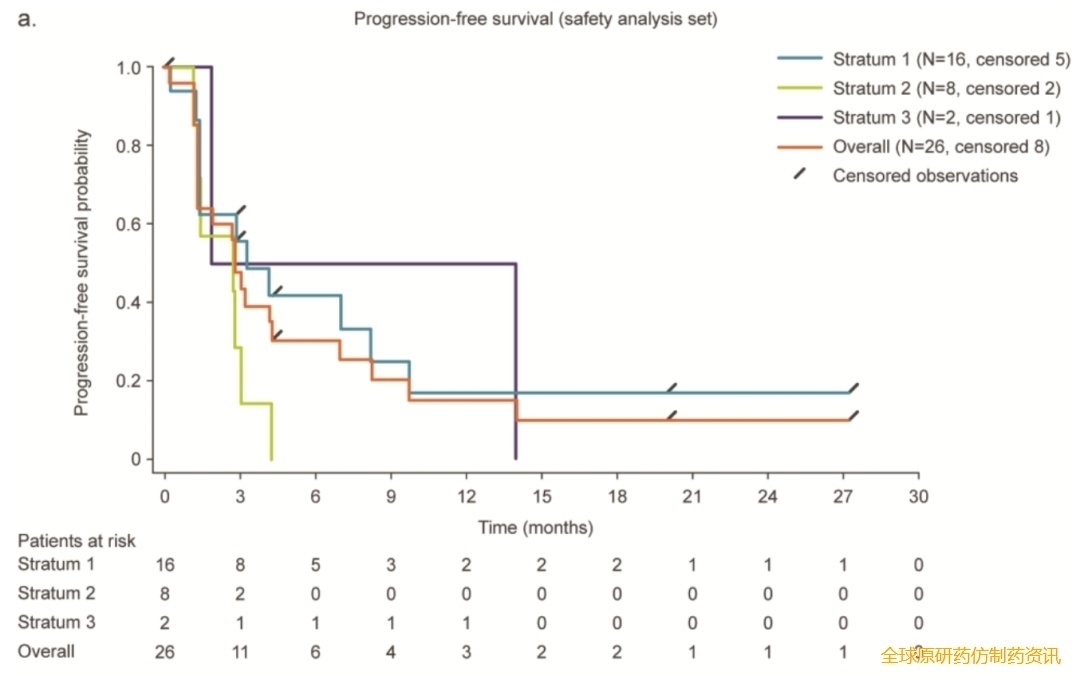
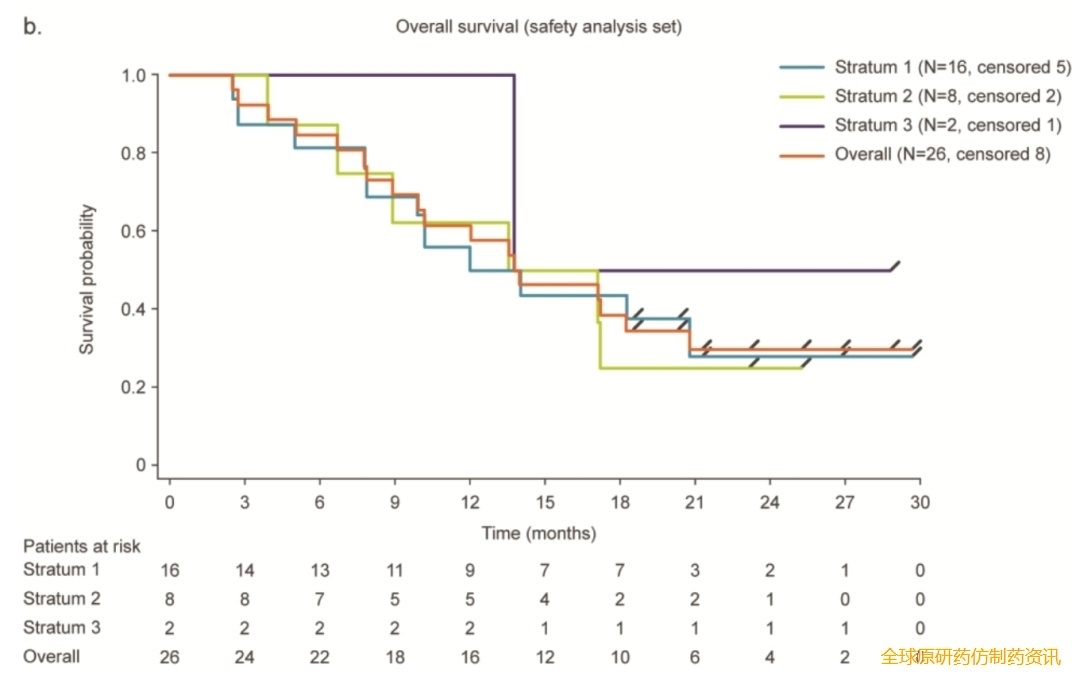
▲图源“PMC”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,BI1361849联合局部放射治疗(可联合或不联合培美曲塞)不仅耐受性良好,还能检测到抗原特异性免疫反应,印证了癌症疫苗联合疗法的潜力。
作为新型抗癌疗法的代表,癌症疫苗历经数十载发展,已从早期基础研究逐步迈向临床试验阶段,更已有古巴肺癌疫苗等正式获批产品问世——其将患者5年生存率从0提升至23%,尽显临床价值。今年,俄罗斯也即将推出一款mRNA癌症疫苗,其初步临床试验已证实100%有效且安全。阅读原文了解详情:100%有效性刷屏!俄罗斯mRNA疫苗早期数据亮眼,全球抗癌潮势不可挡,横扫六大癌种。
而我国在癌症疫苗领域同样成果频出,多款候选疫苗处于火热研发阶段。以针对肝细胞癌的LK101为例,其首次人体临床研究(NCT03674073)中,12名入组患者生存期均超过4年!种种进展无不表明,癌症疫苗已离我们越来越近,“打一针唤醒免疫系统,重新识别并杀伤癌细胞”的设想,或将很快从愿景变为现实,而非遥不可及的天方夜谭!
更振奋人心的是,我国目前已有多款癌症疫苗临床试验陆续开展,且正式启动患者招募。有意向参与的癌友,可将治疗经历、近期病理检查结果等,提交给我们,了解详细入排标准并进行初步评估。


参与临床试验,获取国际前沿新药免费使用机会!更有一线专家团队为你的治疗保驾护航!
相关免费临床招募
PS.如果你正在寻找新药临床项目,欢迎扫码添加微信咨询,帮你少走冤枉路,不花冤枉钱,也欢迎转发给身边其他病友~
新药免费临床招募,推荐有礼!
全国各地临床项目,招募初中晚期肿瘤治疗失败、复发、转移、耐药的患者可入组,免费靶向、免疫、化疗、基因、cart治疗,慢性病(牛皮癣、强直性脊柱炎、糖尿病、高血压、高血脂、荨麻疹、斑秃、脑梗等)、白血病患者免费治疗,如果身边有认识这些病友,可以把这个好消息告诉他们,你的一句转达或许可以挽救一条生命。
主要排除条件
1、使用研究药物首次给药前4周内接受过重大手术的患者或研究期间需要进行重大手术者;
2、有严重的内科疾病,比如严重的心脏病,控制不稳定的高血压,不稳定的传染病(如乙肝)或主要器官功能异常。
※ 以上为受试者入选排除标准的部分主要内容,全面的入组判定标准由研究医生根据研究方案要求详细确认。
患者获益
1、研究期间所使用的试验药物和相关检查检验均免费;
2、根据完成的访视与采血提供一定的交通和营养补偿。
联系咨询电话:187 4940 1825
全球药品资讯论坛微信号:qqyyyfzyzxlt
病历发送邮箱:zzhfzy@sohu.com
如您身边有合适的患者,欢迎推荐
报名成功后,招募人员会在3个工作日与您取得联系
[1]Liau L M,et al.First results on survival from a large Phase 3 clinical trial of an autologous dendritic cell vaccine in newly diagnosed glioblastoma[J]. Journal of translational medicine, 2018, 16(1): 142.
https://translational-medicine.biomedcentral.com/articles/10.1186/s12967-018-1507-6
[2]Wainberg ZA,et al.Lymph node-targeted, mKRAS-specific amphiphile vaccine in pancreatic and colorectal cancer: phase 1 AMPLIFY-201 trial final results. Nat Med. 2025 Aug 11.
https://www.nature.com/articles/s41591-025-03876-4
[3]Lopez J,et al.Autogene cevumeran with or without atezolizumab in advanced solid tumors: a phase 1 trial[J]. Nature Medicine, 2025: 1-13.
生成海报
 长按扫码关注公众号
长按扫码关注公众号