前言
胃癌是全球第五大常见癌症。据统计,我国胃癌患者中32.33%存在肝转移,16.56%存在腹膜转移,且随着疾病进展,5年生存率逐渐降低1。近年免疫治疗革新了胃癌诊疗格局,但免疫单抗疗效仍有待突破,同时靶向PD-1/PD-L1和其它免疫逃逸通路的双抗研发则有望突破局限,实现免疫治疗升级。
在此背景下,2024年ESMO大会披露的SHR-1701-Ⅲ-307研究以扎实的循证医学证据给出了亮眼解答2。2025 ESMO Asia大会进一步公布了其PD-L1 CPS≥1晚期胃癌的亚组分析,结果显示,相较安慰剂联合化疗,瑞拉芙普α(SHR-1701)联合化疗一线治疗PD-L1 CPS≥1晚期胃癌患者在mOS的绝对值和提升上(16.7个月 vs. 10.3个月)均实现突破性进展,死亡风险直降43%,成功突破既往单抗疗效瓶颈,彰显了二代免疫治疗令人鼓舞的疗效3。
2025年ESMO IO大会上,SHR-1701-Ⅲ-307研究的高危特征患者亚组分析以口头报告形式再度亮相,其结果显示,在ITT肝转移人群和PD-L1 CPS≥1肝转移人群中,瑞拉芙普α(SHR-1701)联合化疗一线治疗的mOS相较安慰剂联合化疗分别提升6.5个月和7.2个月(ITT人群:16.8个月 vs.10.3个月,HR=0.46;PD-L1 CPS≥1人群:16.9个月 vs. 9.7个月,HR=0.41),死亡风险降低50%以上,生存获益优异4。并且,本次ESMO IO大会以电子壁报形式公布的一项涵盖该研究在内的11项随机对照研究、8种治疗方案的Meta分析证实,瑞拉芙普α(SHR-1701)联合化疗一线治疗晚期胃癌肝转移的死亡风险降低幅度(OS HR值)优于其他治疗方案。上述研究共同表明瑞拉芙普α(SHR-1701)联合化疗的生存获益不仅显著优于安慰剂联合化疗,且死亡风险降低幅度优于以往PD-(L)1单抗联合化疗方案,为晚期胃癌尤其是肝转移患者带来更优治疗选择和新的循证参考5。
值此良机,医脉通特邀北京大学肿瘤医院彭智教授接受采访,深度剖析瑞拉芙普α(SHR-1701)联合化疗的疗效和安全性,并探讨该方案对重塑胃癌诊疗格局的重要意义。
彭智教授:
晚期胃癌的核心诊疗目标就是延长患者生存期并改善生活质量,但我国胃癌患者人群基数庞大,且晚期胃癌患者占比高、治愈率偏低,生存预后较差,疾病诊疗形势严峻。近年来,国内学者已开展多项针对性研究,其中北京大学肿瘤医院沈琳教授牵头的全国性大规模真实世界研究(涵盖22万例中国胃癌患者)数据显示,肝转移是晚期胃癌最常见的血行转移部位,发生率为32.33%,且此类患者预后较差,生存期显著缩短1。
当前,无论是基于分子分型还是临床特征,胃癌肝转移的诊疗均缺乏明确的特异性策略,其临床诊疗标准尚未完全确立。同时目前指南共识对肝转移患者也尚无特定治疗方案推荐,通常建议进行常规免疫治疗或参加免疫治疗/靶向治疗临床试验,但其获益相对有限。既往研究显示,胃癌肝转移患者的mPFS仅4.9个月,显著劣于无肝转移患者(8.7个月 vs. 4.9个月,P=0.026)6。同时,相较于淋巴结、腹膜或肺转移,免疫单抗治疗后肝转移患者的疾病进展率最高,达57%7。
不同转移部位的胃癌患者预后差异,可能与肿瘤分子生物学行为异质性及免疫微环境的个体化特征密切相关。未来有必要协同革新医疗技术与研发ADC、双抗等新型药物,深入探索针对该类患者的有效标准治疗方案,进而改善生存结局。
彭智教授:
尽管肝转移、腹膜转移或弥漫型等具有特定疾病特征的患者预后相对较差,但SHR-1701-Ⅲ-307研究的亚组分析显示,瑞拉芙普α(SHR-1701)联合化疗方案不仅在全人群中展现出明确疗效优势,在预后不佳的转移亚组中同样实现了显著的生存获益,且该获益随PD-L1表达水平的升高呈增强趋势4。
2025年 ESMO IO大会披露的数据显示,在肝转移患者群体中,无论ITT人群(16.8个月 vs 10.3个月,HR=0.46)还是PD-L1 CPS≥1(16.9个月 vs 9.7个月,HR=0.41)亚组,瑞拉芙普α(SHR-1701)联合化疗均带来了显著的OS获益,患者死亡风险降低超50%4。这提示,瑞拉芙普α(SHR-1701)联合化疗方案能够显著改善肝转移患者生存,为破解此类患者的治疗困境提供了关键依据,具有重要的临床价值,有望改变晚期胃癌肝转移患者一线治疗的格局。
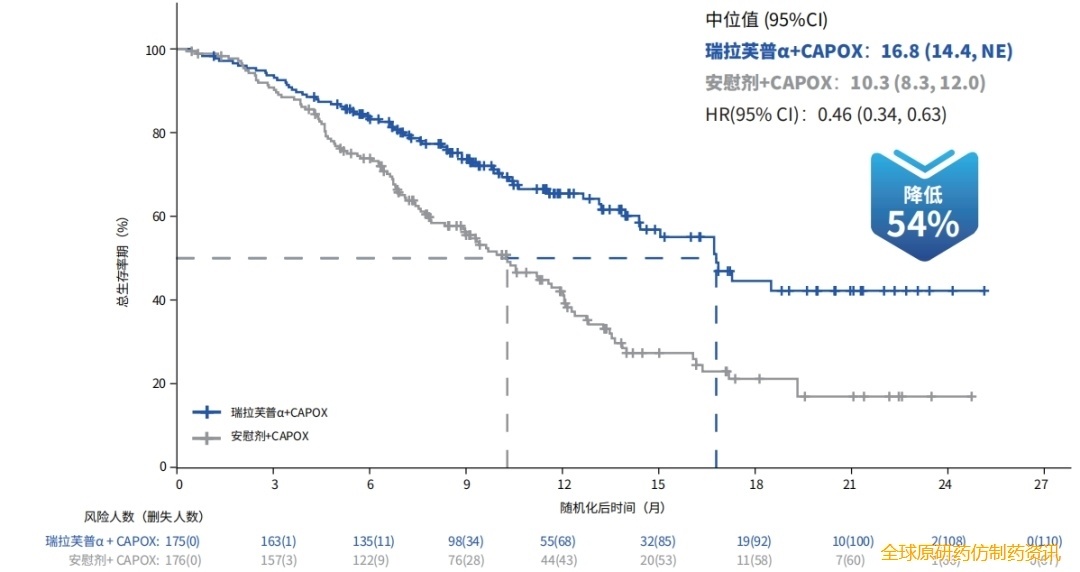
图 1 SHR-1701-Ⅲ-307研究中ITT人群肝转移亚组OS分析(数据来源于2025 ESMO IO. Slides 243MO.)
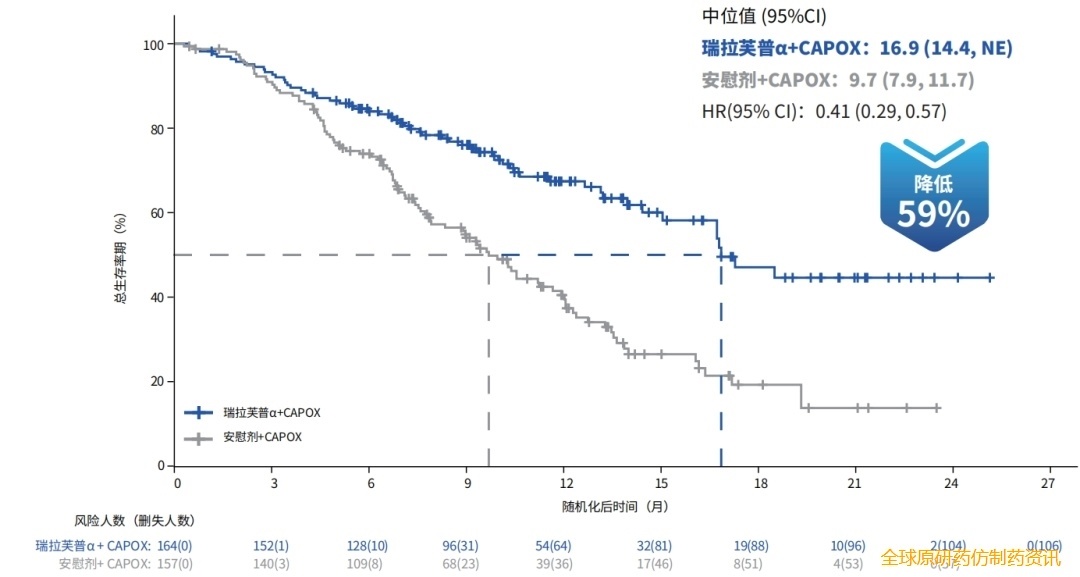
图 2 SHR-1701-Ⅲ-307研究中PD-L1 CPS≥1人群肝转移亚组OS分析(数据来源于2025 ESMO IO. Slides 243MO.)
同样于本次大会上披露的Meta分析将其与同类研究进行横向对比。该研究共纳入11项随机对照研究,呈现了8种治疗方案(7种免疫+化疗方案和1种CLDN18.2靶向+化疗方案)相较于单纯化疗的疗效与安全性。最终结果显示,瑞拉芙普α(SHR-1701)联合化疗在肝转移人群中呈现出更优的HR(0.46)5。该研究不仅有力验证了瑞拉芙普α(SHR-1701)联合化疗的疗效优势,更证实其有望突破传统单抗的疗效瓶颈,打破胃癌肝转移患者的生存困境,成为此类患者未来临床治疗的优选方案。
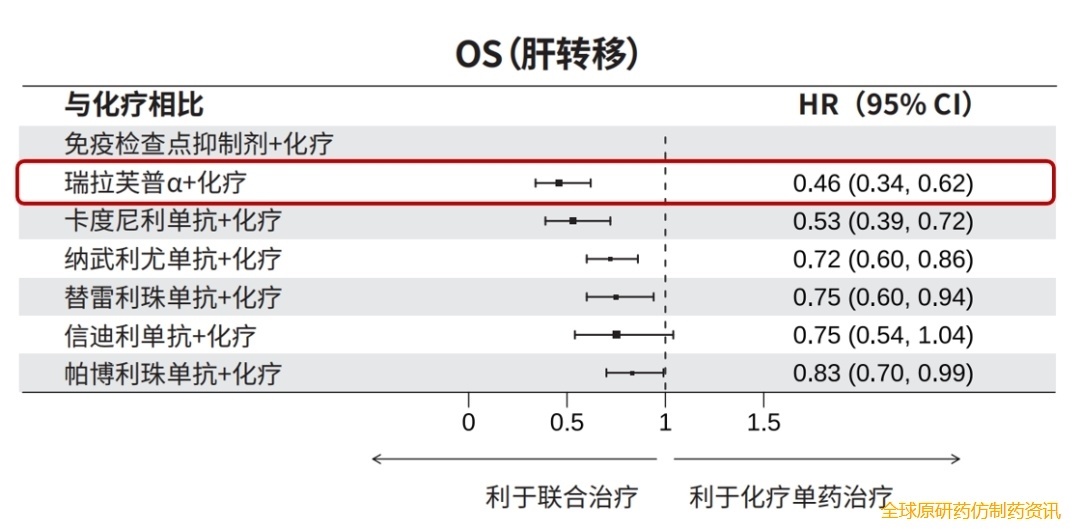
图 3 Meta分析的ITT人群肝转移亚组结果(数据来源于2025 ESMO IO. Poster 320eP)
在腹膜转移患者中,研究显示,瑞拉芙普α(SHR-1701)联合化疗在ITT人群(12.6个月 vs 8.4个月,HR=0.68)和PD-L1 CPS≥1人群(12.7个月 vs 8.3个月,HR=0.58)中生存获益显著。在弥漫型胃癌这种预后极差的亚型中,瑞拉芙普α(SHR-1701)联合化疗同样表现出一致的生存优势(ITT人群:16.4个月 vs 9.5个月,HR=0.50;PD-L1 CPS≥1人群:16.4个月 vs 8.3个月,HR=0.38),死亡风险降低超过50%4。这表明,通过同时阻断PD-L1与TGF-β双通路,该联合方案为高危难治性人群治疗提供了高级别循证医学证据和更优的治疗选择。
因此,双抗等新型药物的临床研究,为阐释疾病本质、解析肿瘤分子生物学行为及药物作用机制提供了全新视角。未来针对晚期胃癌高危患者的全程管理,临床还需重视个体异质性和强化MDT模式,同步开展疼痛管理等生活质量干预,全方位优化治疗获益,最终改善患者生存。
彭智教授:
当前免疫检查点抑制剂在胃癌肝转移患者中的治疗效果尚不理想,这一临床现象可能与肝转移灶独特的肿瘤微环境密切相关——该微环境特征可能导致现有抗PD-1/PD-L1单抗治疗的应答率偏低。
瑞拉芙普α(SHR-1701)作为PD-L1/TGF-β双特异性抗体融合蛋白,双重通路激活免疫系统,增强肿瘤杀伤效应。在胃癌肝转移的肿瘤微环境中,抑制TGF-β通路能够发挥多重调控作用:促进CD8+T细胞增殖与募集,提高肝转移灶内活性CD8+T细胞的比例,减少Treg数量并抑制肿瘤相关成纤维细胞(CAFs)的活性及功能,增强CD8+T细胞浸润肿瘤,由此扭转肝转移造成的免疫抑制环境,因此在胃癌肝转移治疗中具有更高的临床潜力和应用价值8-11。基于这一独特机制,瑞拉芙普α(SHR-1701)在高危人群中的疗效优势已在SHR-1701-Ⅲ-307研究中得到了充分验证。
未来临床将持续推进相关基础研究,深入探索其作用机制,为胃癌肝转移患者提供更具针对性的新型治疗方案。
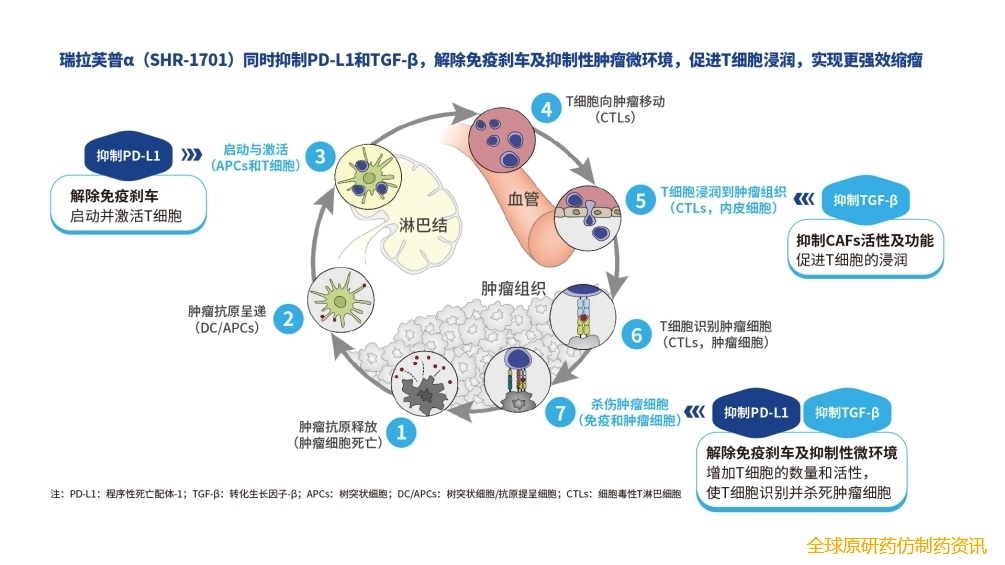
图 4 瑞拉芙普α(SHR-1701)的作用机制
彭智教授:
当前国内晚期胃癌一线治疗领域已涌现多项阳性结果的Ⅲ期临床研究,这为临床诊疗提供了更多选择。2025 ESMO Asia大会披露了瑞拉芙普α(SHR-1701)联合化疗在PD-L1 CPS≥1人群中的亚组分析。结果显示,在HER2阴性晚期胃癌PD-L1 CPS≥1人群中,瑞拉芙普α(SHR-1701)联合化疗的mOS和mPFS分别为16.7个月和7.1个月,相较安慰剂联合化疗分别延长了6.4个月(HR=0.57)和1.6个月(HR=0.51)3。这为瑞拉芙普α(SHR-1701)联合化疗在晚期胃癌PD-L1 CPS≥1人群一线治疗中确立重要地位提供了有力支持。
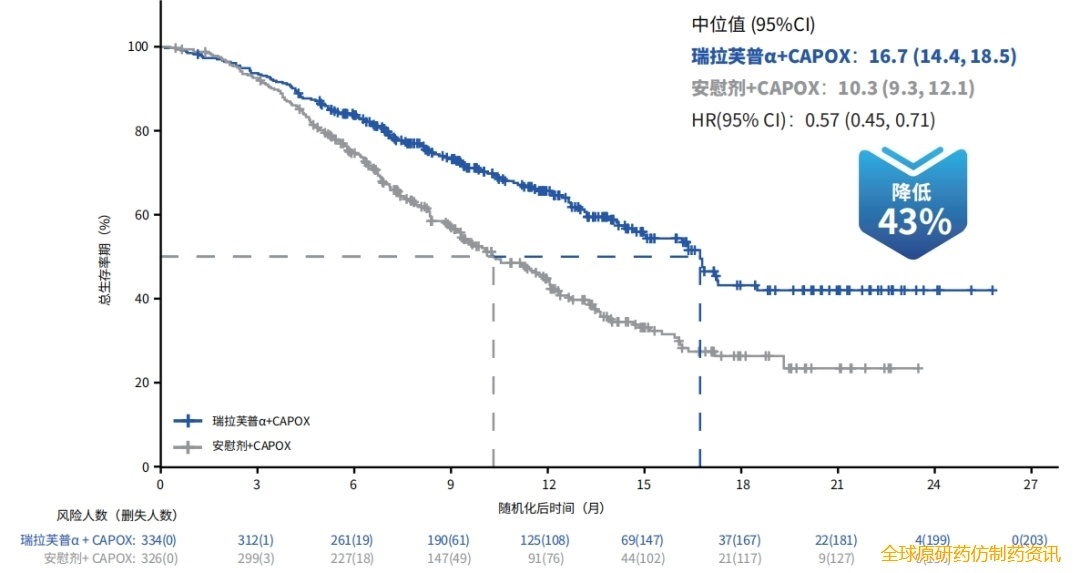
图 5 SHR-1701-Ⅲ-307研究中PD-L1 CPS≥1人群的OS分析(数据来源于2025 ESMO Asia. Poster 298P.)
不过由于尚无头对头的临床研究数据作为直接依据,针对多种经临床研究证实有效的治疗方案,医生与患者往往面临决策困惑。基于此,本次大会公布的Meta分析旨在为临床优化药物组合选择提供参考依据。结果显示,在PD-L1 CPS≥1人群中,和化疗相比,各治疗方案中瑞拉芙普α(SHR-1701)联合化疗展现出显著的OS改善,降低死亡风险43%(HR=0.57),显示出更有利的OS获益趋势。因此,本Meta分析结果表明,与其他各项免疫治疗方案间接比较,瑞拉芙普α(SHR-1701)联合化疗显示更优的OS获益趋势,具有显著的疗效优势与良好的安全性5。
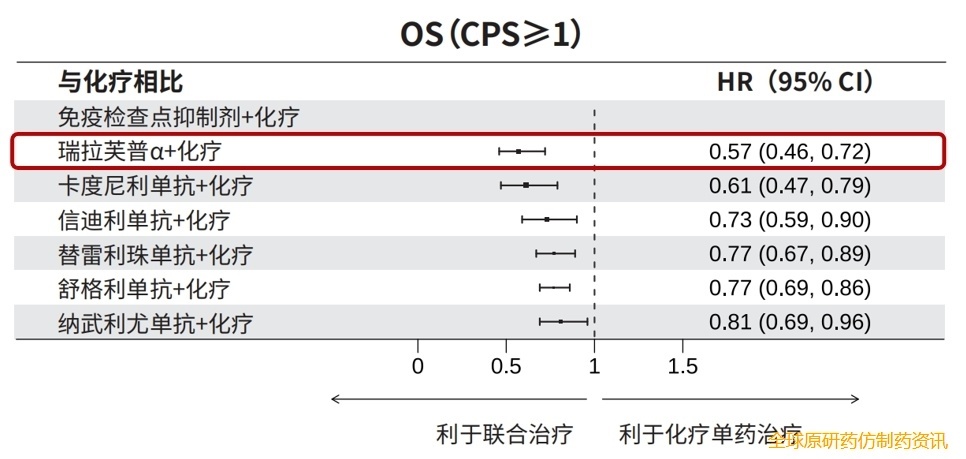
图 6 Meta分析中PD-L1 CPS≥1人群的OS森林图:化疗 vs 各治疗方案(数据来源于2025 ESMO IO. Poster 320eP)
尽管本研究进行的是间接比较,但其仍为临床医生系统认知现有治疗方案、基于统一标准评估胃癌治疗策略提供了高级别循证医学依据,可作为临床决策的重要参考。需注意间接比较存在固有局限性,因此最终治疗方案的制定仍需结合患者个体特征、药物可及性及治疗意愿综合考量。
凭借协同机制与明确生存优势,瑞拉芙普α(SHR-1701)联合化疗能够显著改善晚期胃癌PD-L1 CPS≥1患者生存结局,成为改变晚期胃癌治疗格局的关键突破。本次ESMO IO大会披露的两项研究结果充分证实,瑞拉芙普 α(SHR-1701)联合化疗方案可显著延长晚期胃癌肝转移患者的生存期,且相较于其他免疫治疗策略,该联合疗法能够为此类患者带来更具临床优势的生存获益。期待未来随着相关研究的不断深入和临床经验的持续积累,这一创新方案能让更多晚期胃癌患者获得长期生存,推动我国胃癌诊疗水平迈向新台阶。
彭智 教授
北京大学肿瘤医院
博士,博士生导师
北京大学肿瘤医院主任医师,北京大学博雅青年学者
国家级青年人才项目获得者
中国抗癌协会胃癌专委会委员
中国抗癌协会肿瘤转移专委会委员
中国抗癌协会肿瘤精准治疗委员会委员
CSCO胃癌专家委员会委员兼秘书
CSCO肿瘤营养治疗专家委员会委员
中国免疫学会临床免疫分会委员
北京癌症防治学会胃癌防治专委会主委
北京癌症防治学会消化道精准治疗专委会副主任委员
《中华医学杂志》《肿瘤综合治疗电子杂志》编委
获得中华医学会一等奖、中国抗癌协会青年科学家奖、中国抗癌协会一等奖等
参考文献
1.Chen Y, et al. J Hematol Oncol. 2025 Apr 15;18(1):42.
2.Shen L, et al. 2024 ESMO LBA60.
3.Peng Z, et al. 2025 ESMO Asia. Poster 298P.
4.Peng Z, et al. 2025 ESMO IO. Slides 243MO.
5.Peng Z, et al. 2025 ESMO IO. 320eP.
6.Liang H, et al. Front Immunol. 2022 Sep 21:13:1015549.
7.Kadono T, et al. Cancer Med. 2023 Apr;12(8):9322-9331.
8.Boussiotis VA. N Engl J Med. 2016;375(18):1767-1778.
9.Henriques A, et al. Nature Genetics, 2025: 1-16.
10.NCI-Immune Checkpoint Inhibitors. Available at:
https://www.cancer.gov/about-cancer/treatment/types/immunotherapy/checkpoint-inhibitors.
11.Gulley JL, et al. Mol Oncol. 2022;16(11):2117-2134.
审批编号:TG - 肿瘤-胃肠食管SHR-1701: PD-L1/TGF-βRII - 1292 - 2028-11
撰写:Astra
审校:Babel
排版:Atai
执行:Squid
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
生成海报
 长按扫码关注公众号
长按扫码关注公众号